肺癌是呼吸系统恶性肿瘤之一,恶性致死性高,预后差。根据《全球癌症统计》(Global Cancer Statistics), 2020年全球肺癌新发病例将达到2 206 771例,死亡病例将达到1 796 144例,其中死亡病例占新发病例的80%以上,在全球癌症死亡原因中排名第二,在中国排名第一,预计到2030年将升至美国第一。与此同时,超过90%的肺癌患者被诊断为晚期,往往错过了最佳治疗时机,5年生存率仅为约10%-20%。5迄今为止,肺癌的主要治疗策略仍然是手术切除联合辅助治疗,但只有20%的患者适合手术,80%的患者术后复发并最终死亡。因此,寻求一种新的治疗策略来阻止肿瘤进展,延长肺癌患者的生存时间是非常重要的。
越来越多的证据表明,免疫疗法,特别是单克隆抗体靶向药物,已越来越多地用于肺癌的临床治疗,但仍有许多局限性。有趣的是,临床研究表明,嵌合抗原受体(CAR - T)细胞作为一种超顶级T细胞免疫疗法,首先从患者血液中分离T细胞,对T细胞进行基因工程改造,使其识别肿瘤细胞上的抗原并杀死它们,被认为是一种安全可靠的恶性肿瘤免疫疗法。目前,CAR - T细胞免疫疗法在血液系统恶性肿瘤治疗中取得了巨大成功,总缓解率达到80%以上。例如,临床试验已经证实靶向CD19的CAR - T细胞对耐药B细胞恶性肿瘤具有持久的缓解作用,对复发和难治性急性B淋巴细胞白血病患者的治愈率约为80%-90%。目前,有5种靶向CD19的CAR - T治疗血液系统恶性肿瘤的产品已经获得美国食品和药物管理局(FDA)的批准,这为癌症免疫治疗和抗肿瘤道路带来了新的方向。同时,CAR - T细胞免疫疗法在血液系统恶性肿瘤治疗中的成功为治愈实体肿瘤提供了新的希望,一系列实体肿瘤CAR - T细胞靶抗原已经被确定并用于正在进行的早期临床试验。一些科学家已经将注意力集中在CAR - T细胞免疫疗法治疗肺癌上,并在临床试验中取得了良好进展。上述研究结果表明,CAR - T细胞免疫疗法可能是治疗肺癌的一种新策略。
CAR - T细胞作为肿瘤免疫治疗的新兴治疗策略之一,成为近年来肿瘤治疗研究的新热点和焦点。CAR-T细胞通过基因工程将患者的T细胞分离到体外,并表达单链抗体,特异性识别并结合癌细胞上的抗原(如CD19)。CAR主要由细胞外抗原识别结构域(ectodomain)、铰链和跨膜结构域以及细胞内信号转导结构域(endodomain)组成。细胞外抗原识别结构域的主要结构是靶抗原抗体的单链可变片段(scFv),它由肿瘤相关抗原(TAA)特异性抗体的重链可变区(VH)和轻链可变区(VL)组成。保留了抗体的识别能力,这种类型的识别确保了T细胞杀伤作用的特异性。铰链和跨膜结构域通常是CD8α或CD28的跨膜区域,主要用于连接细胞外和细胞内结构域,并参与CAR和抗原的相互识别以及CAR - T激活的刺激信号的募集。跨膜结构域的长度或灵活性也会影响CAR的功能。细胞内信号转导结构域主要由刺激因子CD3ζ链组成,通常与CD27、CD28、CD134 (OX‐40)和CD137(4‐1BB)等共刺激分子结合,这些共刺激分子启动T细胞功能的激活,也有助于T细胞增殖和寿命延长。
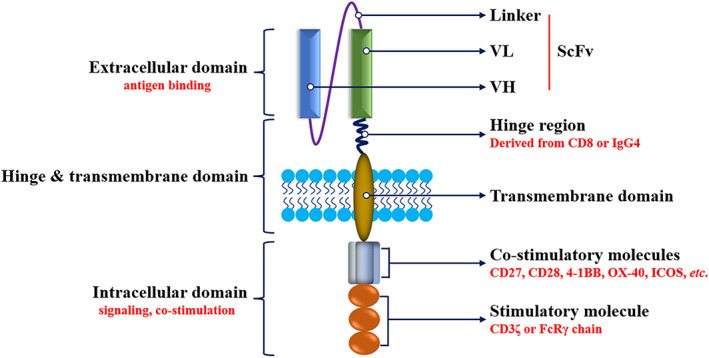
CAR的结构
迄今为止,CAR - T细胞根据其细胞内信号结构域分为五代,CAR - T细胞世代之间的主要差异是特异性共刺激分子。第一代CAR - T细胞仅包括CD3ζ作为细胞内信号内域,与细胞外scFv融合以修饰和激活T细胞。由于第一代CAR - T细胞不具有共刺激分子,因此它们不能长时间触发T细胞活化,因此抗肿瘤作用很小。为了克服这一缺陷,我们将共刺激分子(如CD28、4 - 1BB和诱导共刺激[ICOS])添加到第二代CARs结构中,以增强T细胞的增殖能力。先前的研究表明,CD28 CAR - T细胞在杀死癌细胞方面更有效,而且4 - 1BB CAR - T细胞对癌细胞表现出更低的耗竭率和更持久的杀伤作用。为了提高T细胞的肿瘤杀伤能力,第三代car是在第二代car的基础上继续添加共刺激分子,如CD28与OX - 40/4 - 1BB联合。多项研究表明,第三代CAR - T细胞的细胞因子分泌水平上调,对癌细胞增殖的抑制作用增强。第四代car,也被称为通用细胞因子介导杀伤(truck)的T细胞,增加了编码细胞因子的基因,通过分泌大量炎症细胞因子,如白细胞介素(IL) - 12、IL - 15和粒细胞-巨噬细胞集落刺激因子,进一步激活和招募更多的免疫细胞来对抗免疫抑制的局部肿瘤微环境,这有助于实体肿瘤的免疫治疗。最近的研究指出,第五代car含有IL‐2受体β (IL‐2Rβ)片段,而不是OX‐40/CD27。IL - 2Rβ片段促进肿瘤中Janus激酶、信号转导和转录- 3/5激活因子的水平,但第五代car的安全性和有效性仍在研究中。值得注意的是,复杂过表达片段的构建可能会影响CAR - T细胞的转导效率,甚至加速CAR - T细胞的耗损。迄今为止,第二代CAR - T应用更广泛,效果更稳定。
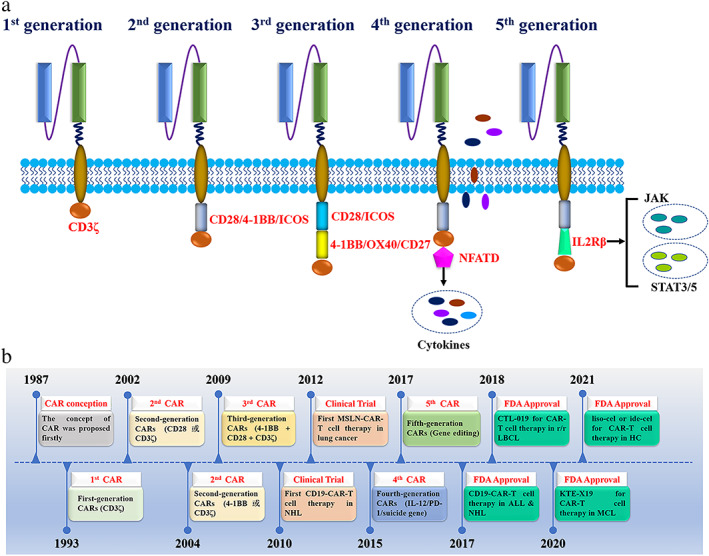
CAR-T的发展史
表皮生长因子受体
大量研究证实,表皮生长因子受体(epidermal growth factor receptor, EGFR)属于生长因子受体酪氨酸激酶的ErbB家族,在许多实体瘤细胞的膜表面高度表达,与肿瘤血管生成、转移和复发有关。Scharpenseel等人证实,EGFR在非小细胞肺癌(NSCLC)(原发肿瘤)和脑转移患者的组织中表达上调。此外,EGFR可作为实体瘤诊断和治疗的有效靶点。重要的是,EGFR已成为多种肿瘤(包括肺癌)基于抗体的免疫治疗的新靶点。一项EGFR阳性的复发/难治性NSCLC临床试验(NCT01869166)的结果显示,抗EGFR CAR - T细胞治疗后,没有患者出现明显的毒副反应,2例患者达到部分缓解(PR), 5例患者病情稳定(SD) 2-8个月。病理活检显示靶向EGFR的CAR - T细胞可以浸润肿瘤组织并诱导EGFR特异性细胞毒性。此外,Zhang等人证实EGFR变体III (EGFRvIII)‐CAR‐T细胞可以通过释放干扰素γ (IFN‐γ)和肿瘤坏死因子α (TNF‐α)等细胞因子,有效识别和杀死EGFRvIII阳性肺癌细胞,并有助于抑制体内移植肿瘤的生长,这表明靶向EGFRvIII的CAR‐T细胞是预防肺癌术后复发和转移的有效治疗策略。另一项I期试验(NCT04153799)证实,使用C‐X‐C趋化因子受体(CXCR) 5型修饰的抗EGFR CAR‐T细胞来评估EGFR阳性NSCLC患者的安全性和可行性。上述研究提示EGFR CAR - T细胞可能通过调节肺癌肿瘤免疫微环境发挥免疫杀伤作用。
Mesothelin
间皮素(MSLN)是一种促进肿瘤侵袭和转移的细胞粘附糖蛋白。MSLN过表达与肺癌患者肿瘤侵袭性高、预后差呈正相关,是恶性胸膜间皮瘤和肺癌的诊断和治疗靶点。据报道,MSLN是实体瘤CAR - T治疗中更理想的TAA。美国国立卫生研究院(NIH)进行了一项早期临床试验(NCT01583686),以测试MSLN - CAR - T细胞治疗晚期恶性肿瘤(包括肺癌、胰腺癌、恶性间皮瘤、宫颈癌和卵巢癌)的安全性和可行性。结果显示,共入组15例I期临床试验患者的严重不良反应发生率为40%(6/15),其中贫血、血小板减少、便秘和低氧血症各1例,淋巴细胞减少2例,而在3.5个月的观察期内,只有1例患者病情稳定(SD)。体内实验表明,在非小细胞肺癌中,MLSN - CAR - T细胞通过表现出比T细胞更高的杀伤癌细胞的能力来抑制异种移植物的生长。另一项研究证实,MSLN - CAR - T细胞治疗通过胸部注射显著抑制肿瘤生长,并在小鼠体内持续很长时间。此外,靶向MSLN和癌胚抗原(CEA)抗原的双CAR - T细胞具有更强的抗胰腺癌活性。综上所述,MSLN可能是CAR - T细胞在实体瘤免疫治疗中的有效TAA。
粘蛋白1
Mucin 1 (MUC1)是一种促进癌细胞粘附和转移的跨膜蛋白。既往研究证实MUC1在肺癌组织中的表达明显高于正常肺组织。另一项研究表明,在体外实验中,敲低MUC1可显著抑制肺癌细胞增殖和诱导凋亡,并抑制原位肺癌小鼠模型中肿瘤的生长和转移。值得注意的是,MUC1已被报道为小细胞肺癌免疫治疗的可靠靶点。 Wei等研究表明,靶向前列腺干细胞抗原(PSCA)和MUC1的CAR - T细胞可显著消除NSCLC中PSCA和MUC1联合阳性的肿瘤细胞。上述研究表明,抗MUC1 CAR - T细胞可能是肺癌患者免疫治疗的有效策略。
酪氨酸蛋白激酶跨膜受体
酪氨酸蛋白激酶跨膜受体(ROR1)是一种酪氨酸激酶样孤儿受体,在B细胞慢性淋巴母细胞白血病、套细胞淋巴瘤、急性淋巴细胞白血病、肺癌、乳腺癌、胰腺癌和卵巢癌中表达上调,但在正常组织中表达极低。Fred Hutchinson癌症研究中心(NCT02706392)的一项临床试验评估了抗ROR1 CAR - T细胞治疗晚期ROR1阳性和IV期非小细胞肺癌和三阴性乳腺癌(TNBC)的效果,结果显示,招募的30名患者中至少有6名没有表现出剂量限制性毒性。Wallstabe等人通过三维肿瘤模型证明,用抗ROR1 CAR - T细胞治疗可以有效地杀死NSCLC和TNBC细胞。因此,靶向ROR1的CAR - T细胞为肺癌的临床治疗提供了一种新的策略。
人表皮生长因子受体2
先前的研究证实,人表皮生长因子受体2 (HER2)在肺癌中高表达,促进癌细胞的增殖、侵袭和血管生成。HER2是一种很有前景的肺癌诊断和治疗生物标志物。Zhao等人报道了抗HER2 CAR - T细胞在异种小鼠模型中对HER2阳性肿瘤表现出抗肿瘤作用。此外,国内外许多学者正在开展抗HER2 CAR - T细胞治疗肺癌的临床试验,以验证HER2 - CAR - T细胞治疗HER2阳性肺癌的安全性和有效性。
程序性死亡-配体
CAR - T细胞治疗非小细胞肺癌的疗效与免疫抑制肿瘤微环境有关。程序性死亡配体1 (Programmed death‐ligand 1, PD‐L1)是一种重要的免疫检查点,在多种肿瘤中表达上调,它可以通过与T细胞上的PD‐1结合抑制T细胞的增殖和活化,最终导致肿瘤细胞的免疫逃逸。先前的研究表明,PD‐L1抗体在体外、体内实验和肿瘤(包括肺癌)的临床试验中表现出安全且令人兴奋的结果。此外,CAR - T细胞靶向PD - L1和zeusshield细胞毒性T淋巴细胞的安全性和有效性正在一项正在进行的用于复发或难治性NSCLC (NCT03060343)的早期I期试验中进行评估。Liu等人证明抗PD‐L1 CAR‐T细胞显著抑制PD‐L1高NSCLC细胞增殖和异种移植肿瘤的生长,同时放射治疗联合抗PD‐L1 CAR‐T细胞对PD‐L1低NSCLC细胞和异种移植肿瘤表现出细胞毒性活性。然而,由于严重不良事件(NCT03330834),一项针对晚期肺癌的抗PD‐L1 CAR‐T细胞免疫疗法的I期临床试验被终止。有趣的是,在一项II期试验(NCT03525782)中,使用抗MUC1 CAR - T联合PD - 1敲低细胞来评估晚期NSCLC患者的安全性和有效性。
总的来说,CAR-T细胞疗法在血液系统恶性肿瘤中的成功,为肺癌的临床治疗带来了新的希望,并进入了快速发展阶段。但是大量临床试验进展缓慢,疗效非常有限,还有几个技术瓶颈需要解决。与血液系统恶性肿瘤不同,CAR - T细胞治疗肺癌的几个主要挑战包括靶向/肿瘤外毒性、TAA异质性、免疫抑制肿瘤微环境(TME)、神经毒性、细胞因子释放综合征等。如何克服这些挑战是目前CAR - T细胞治疗肺癌的热点领域。
文章转载自《PMC》
目前免疫管家已开通微信公众号,健康界,知乎,今日头条等多自媒体网站并且同名[免疫管家]
扫描下方二维码,或者直接电话咨询免疫管家医学部(400-880-3716),为癌友患者们分享更多信息。

免责声明:免疫管家为免疫科普平台,文本参考来源于网络,版权归原作者所有。该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!
相关推荐
随便看看
- GPRC5D靶向CAR-T细胞治疗骨髓瘤
- 基于全人源纳米抗体的工程化CAR T细胞增强了对肝细胞癌的抗肿瘤活性。
- CD19 CAR-T 细胞治疗 B 细胞恶性肿瘤:系统评价和荟萃分析,重点关注 CAR 结构域、制造条件、细胞产物、剂量、患者年龄和肿瘤类型的临床影响
- CD38靶向CAR-T细胞疗法:同种异体造血干细胞移植后复发性急性髓系白血病的新型免疫治疗策略
- CD166特异性CAR-T细胞有效靶向结直肠癌细胞
- CAR-T细胞治疗泌尿系统肿瘤:现在和未来
- CAR-T细胞联合mRNA疫苗治疗实体瘤
- b细胞成熟抗原与CD19嵌合抗原受体T细胞联合治疗多发性骨髓瘤的长期随访研究
- 靶向CAR-T疗法的新型GUCY2C:在晚期结直肠癌中的疗效。
- CAR-T细胞治疗过程











