作者:小编
更新时间:2024-06-12
点击数:

5月末,美国食品药品监督管理局(FDA)授予inavolisib(GDC-0077,伊那利塞)联合哌柏西利(palbociclib)和氟维司群突破性疗法认定,用于治疗完成内分泌辅助治疗后12个月内或之后复发的PIK3CA突变、激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)的局部晚期或转移性乳腺癌患者。

截图来源于“参考资料1”
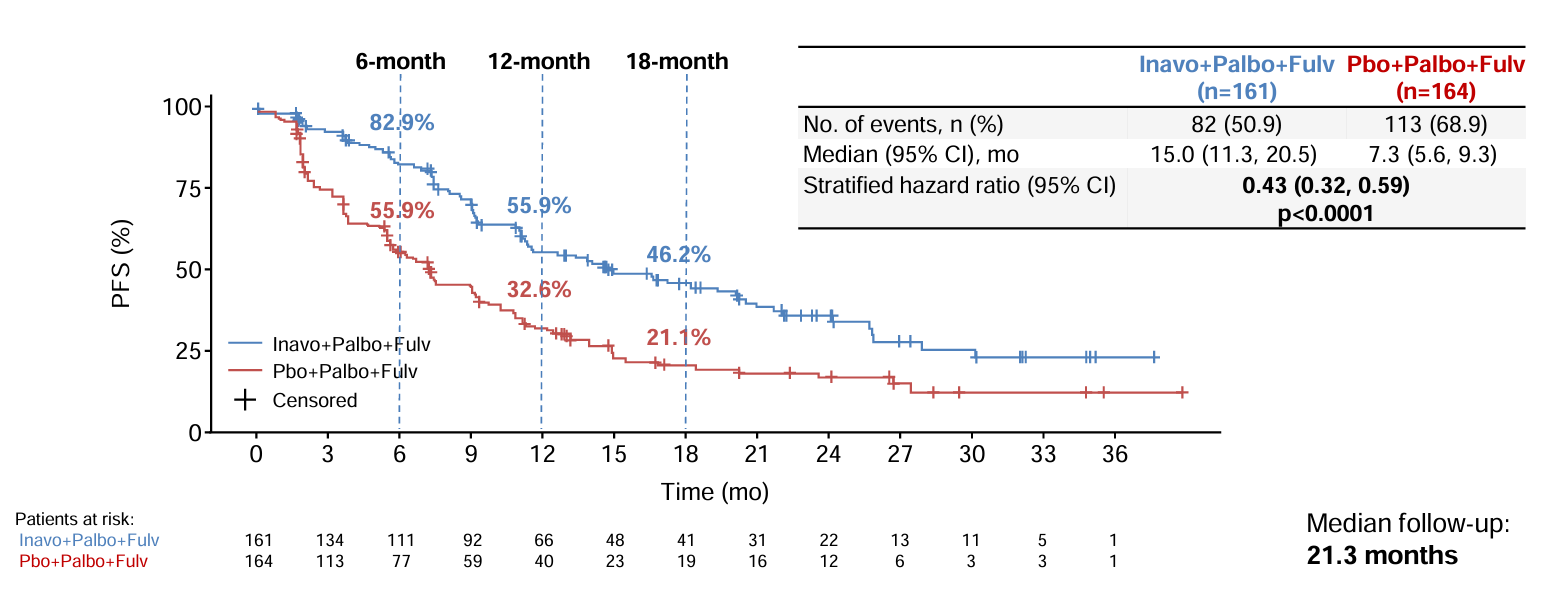
此次认定基于3期INAVO120试验(NCT04191499)的结果。INAVO120试验旨在比较inavolisib (GDC-0077,伊那利塞)联合哌柏西利(palbociclib)和氟维司群与 哌柏西利(palbociclib)和氟维司群的疗效和安全性。共有325名患者被随机分配到研究组(n = 161)或对照组(n = 164) 。
结果显示:在中位随访21.3个月时,inavolisib组的中位无进展生存期(PFS)为15.0个月,而对照组为7.3个月,意味着疾病进展或死亡风险降低了57%!

![]()
参考资料
1.Inavolisib Receives FDA Breakthrough Therapy Designation for PIK3CA-Mutated, HR+/HER2– Breast Cancer (onclive.com)
2.SABCS-2023-presentation-jhaveri-inavolisib-or-placebo-in-combination-with-palbociclib.pdf (roche.com)



相关推荐
随便看看
- 维迪西妥单抗实现HER2阳性乳腺癌患者肿瘤缩小!并拟纳入优先审评
- 注射用西罗莫司(白蛋白结合型)拟纳入突破性疗法
- 重磅!AK112治疗实体瘤研究结果出炉!疾病控制率达63.8%!
- 肿瘤控制率达71%!广谱抗癌药拉罗替尼治疗NTRK融合阳性胃肠道癌效果格外惊艳!
- 欧盟委员会批准特瑞普利单抗治疗鼻咽癌和食管鳞癌
- ADC药物JSKN003获美国FDA授予孤儿药资格认定
- 疾病控制率高达92.0%!赛沃替尼新适应症上市申请已获国家药监局受理
- 全球首款!我国自主研发的首款MEK抑制剂妥拉美替尼国内获批上市!黑色素瘤治疗新选择
- 康宁杰瑞HER2双抗偶联药物(ADC)JSKN003的多项临床研究数据登2025 ASCO
- epaldeudomide (KPG-818) 最新研究成果即将亮相2025 ASH











