
3月28日,和黄医药宣布赛沃替尼用于治疗间质-上皮转化因子 (MET)外显子14跳变的局部晚期或转移性非小细胞肺癌成人患者的新适应症上市申请已获中国国家药品监督管理局受理。若取得批准,赛沃替尼在中国新的标签适应症将扩展至覆盖初治患者。
关于赛沃替尼
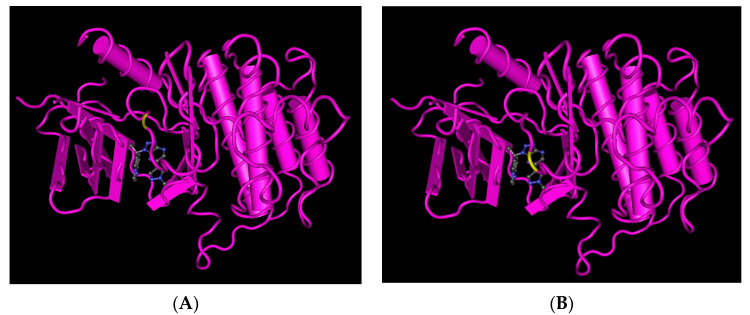
赛沃替尼是一种强效、高选择性的口服MET酪氨酸激酶抑制剂,在晚期实体瘤中表现出临床活性。赛沃替尼可阻断因突变 (例如外显子14跳跃突变或其他点突变)、基因扩增或蛋白质过表达而导致的MET受体酪氨酸激酶信号通路的异常激活。
2021年6月,国家药品监督管理局(NMPA)批准和记黄埔医药(上海)有限公司申报的1类创新药赛沃替尼片(商品名:沃瑞沙/ORPATHYS)上市,用于含铂化疗后疾病进展或不耐受标准含铂化疗的、具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌成人患者。
赛沃替尼自2023年3月1日起获纳入国家医保药品目录,用于治疗含铂化疗后疾病进展或不耐受标准含铂化疗的MET外显子14跳跃突变的局部晚期或转移性非小细胞肺癌成人患者。
IIIb 期确证性研究 (NCT04923945) 的一线治疗队列的初步疗效和安全性数据已于2023年9月在国际肺癌研究协会(IASLC)主办的世界肺癌大会(WCLC)上公布。该IIIb期确证性研究的最终数据已于2024年3月20日在欧洲肺癌大会公布。
这项研究的数据为赛沃替尼作为MET外显子14跳跃突变的初治及经治非小细胞肺癌患者的靶向治疗选择提供了确认性的证据。在初治患者中,独立审查委员会评估的客观缓解率 (ORR)为62.1%,疾病控制率(DCR)为92.0%,中位缓解持续时间 (DoR)为12.5个月。至中位随访时间20.8个月的中位无进展生存期 (PFS)为13.7个月。在经治患者中,独立审查委员会评估的ORR为39.2%、DCR为92.4%、中位DoR为11.1个月。至中位随访时间12.5个月的中位PFS为11.0个月。
目前,赛沃替尼正作为单药疗法或与其他药物的联合疗法,开发用于治疗包括肺癌、肾癌和胃癌在内的多种肿瘤类型。
典型病例
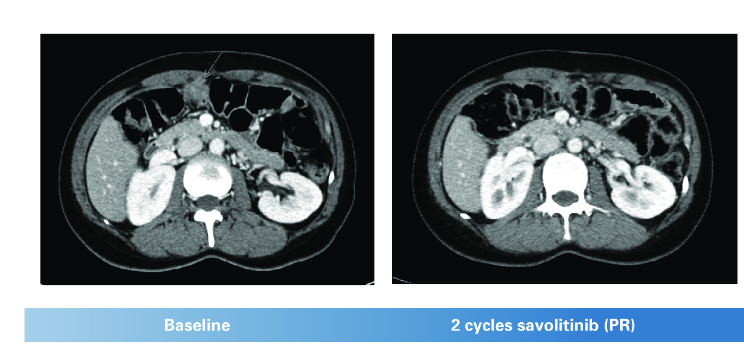
一名31岁的女性,她于2013年因胃癌接受了全胃切除术。患者术后接受放化疗,但18个月后出现双卵巢复发转移。双侧卵巢切除术后,患者术后给予6个周期的卡培他滨加顺铂方案。10个月后,患者出现腹膜播种肿块。之后接受赛沃替尼治疗,治疗期间,她的肿瘤体积减小,部分缓解(PR)达到了6个月,最大直径比基线计算机断层扫描减少了47.7%。
目前医瘤界这里针对赛沃替尼的临床试验正在寻找受试者,想要参加临床试验的患者可通过康和源免疫之家(400-880-3716)进行咨询。

项目名称:赛沃替尼治疗MET基因扩增局部晚期或转移性胃癌和胃食管连接部癌的II期研究(CH1))
部分入选标准:
1.年龄≥18岁;
2.经病理组织学或细胞学诊断的局部晚期或转移性胃癌或胃食道连接部腺癌;
3.MET基因扩增;
4.没有根据RECIST 1.1标准的可测量的胃部以外的病灶,但有可评估病灶。
想要参加临床试验的患者可致电康和源免疫之家医学部(400-880-3716)了解详情后提交病理报告、治疗经历等资料进行初步评估。
扫描下方二维码,或者直接电话咨询康和源免疫之家医学部(400-880-3716),为癌友患者们分享更多信息。

免责声明:康和源免疫之家为免疫科普平台,文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!
参考资料
1.Savolitinib: A Promising Targeting Agent for Cancer - PMC (nih.gov)
2.Mechanisms of Acquired Resistance to Savolitinib, a Selective MET Inhibitor in MET-Amplified Gastric Cancer - PMC (nih.gov)
相关推荐
随便看看
- 美国FDA批准靶向STEAP1的ADC药物ADRX-0405临床试验申请
- Zongertinib的Beamion LUNG-1 Ib期临床研究数据亮相2025 WCLC
- 9MW2821拟纳入突破性治疗
- 塞利尼索片国内第三项适应症获批
- 卡度尼利单抗加含铂化疗联合/不联合贝伐珠单抗在宫颈癌中的III期研究数据公布
- 美国FDA批准阿替利珠单抗新适应症
- EGFR突变非小细胞肺癌新进展,疾病控制率高达100%!
- 匹米替尼(ABSK021)纳入优先审评,用于腱鞘巨细胞瘤
- PC-002获得快速通道资格,用于治疗伯基特淋巴瘤
- cORR达60.8%,我国自主研发的舒沃替尼上市,EGFR 20ins突变的NSCLC的患者获益











