9月24日,君实生物宣布欧盟委员会(EC)批准抗PD-1单抗药物特瑞普利单抗联合顺铂和吉西他滨一线治疗复发、不能手术或放疗的,或转移性鼻咽癌(NPC)成人患者以及联合顺铂和紫杉醇一线治疗不可切除的晚期/复发或转移性食管鳞癌(ESCC)成人患者。
此次批准分别基于III期JUPITER-02研究(NCT03581786)和III期JUPITER-06的研究(NCT03829969)成果。
JUPITER-02是一项随机、双盲、安慰剂对照、国际多中心Ⅲ期临床研究,旨在评估特瑞普利单抗联合吉西他滨-顺铂作为复发性或转移性 NPC 的一线治疗,与单独使用吉西他滨-顺铂相比,是否会显着改善未接受过化疗的复发性或转移性 NPC 患者的无进展生存期和总生存期。2023年《美国医学会杂志》(Journal of the American Medical Association,JAMA)发表了该研究数据结果。
该试验共289例患者接受治疗,其中146例患者接受特瑞普利单抗组治疗,143例患者接受安慰剂组治疗,结果显示:特瑞普利单抗组中位无进展生存期(PFS)比安慰剂组延长了 13.2 个月,分别为21.4 个月和 8.2 个月,1 年无进展生存率分别为 59.0%和 32.9%,2 年无进展生存率分别为44.8%和25.4%。
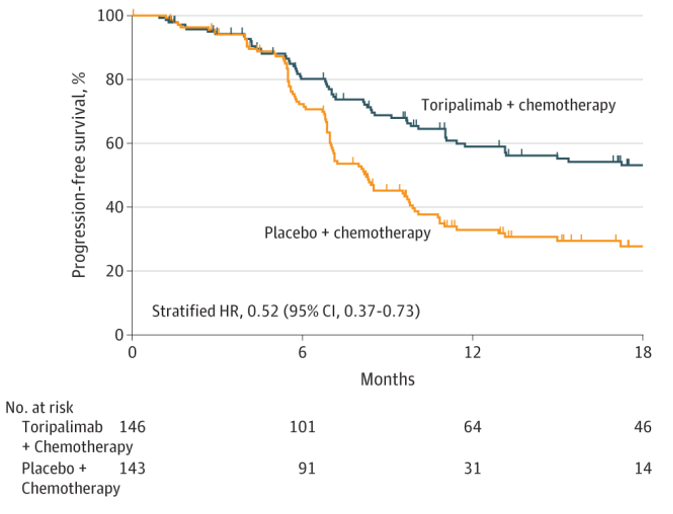
截图来源于参考资料1,侵权请联系删除
特瑞普利单抗组未达到中位总生存期,而安慰剂组为 33.7 个月。特瑞普利单抗组1 年总生存率为 90.9%,安慰剂组为 87.1%,2年总生存率分别为78.0%和65.1%,3年总生存率分别为64.5%和 49.2%。
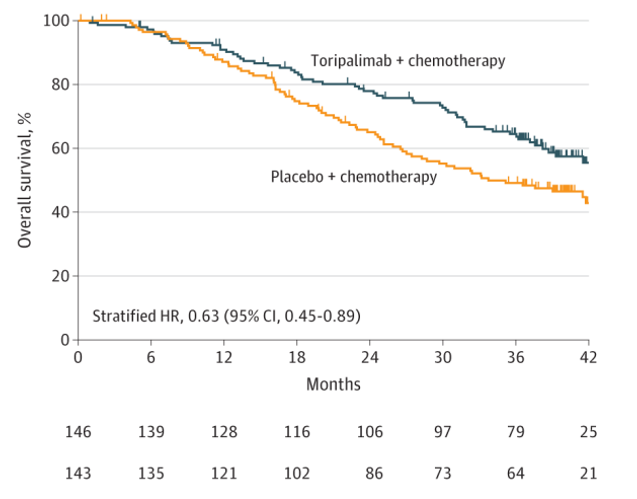
截图来源于参考资料1,侵权请联系删除
特瑞普利单抗组客观缓解率(ORR)为 78.8%,安慰剂组为67.1%。特瑞普利单抗组完全缓解率是安慰剂组的两倍,分别为26.7%和13.3%,也就是说特瑞普利单抗组有39例患者实现完全缓解(CR),安慰剂组是19例患者实现完全缓解。特瑞普利单抗组中位反应持续时间为 18.0 个月,安慰剂组为 6.0 个月。疾病控制率(DCR)分别为88.4%和80.4%。
试验表明,与单独化疗相比,在化疗中加入特瑞普利单抗作为 RM-NPC 的一线治疗提供了具有统计学意义和临床意义的无进展生存期和总生存期获益。
JUPITER-06是一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究(NCT03829969),旨在评估与安慰剂联合化疗相比,特瑞普利单抗联合紫杉醇/顺铂(TP)用于晚期ESCC一线治疗的疗效及安全性。2022年国际顶尖肿瘤学杂志《Cancer Cell》发表了该试验数据。
该试验分别有257例患者接受特瑞普利单抗组和安慰剂组治疗,结果显示:特瑞普利单抗组中位无进展生存期优于安慰剂化疗联合组,分别为5.7个月和5.5个月,去年无进展生存率分别为27.8%和6.1%。
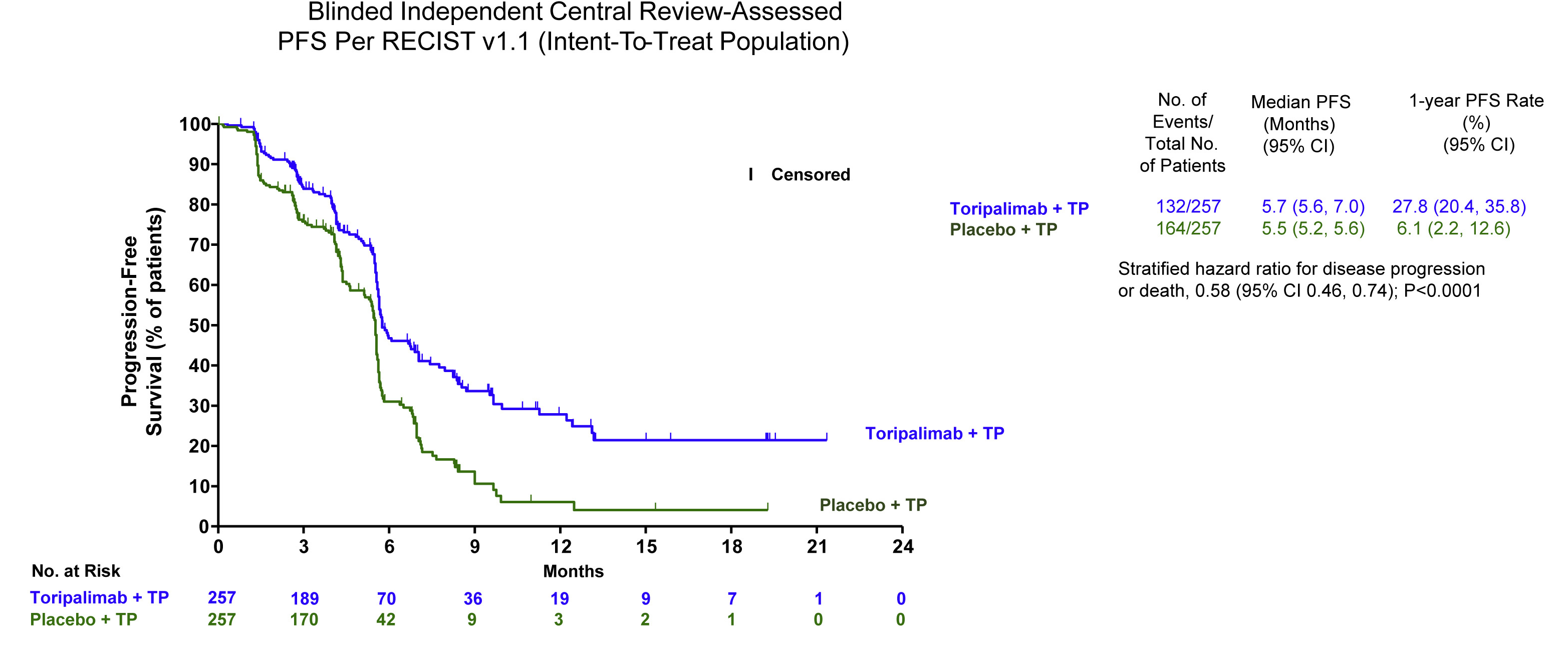
中位总生存期分别为17个月和11个月,1年生存率分别为66.0%和43.7%。
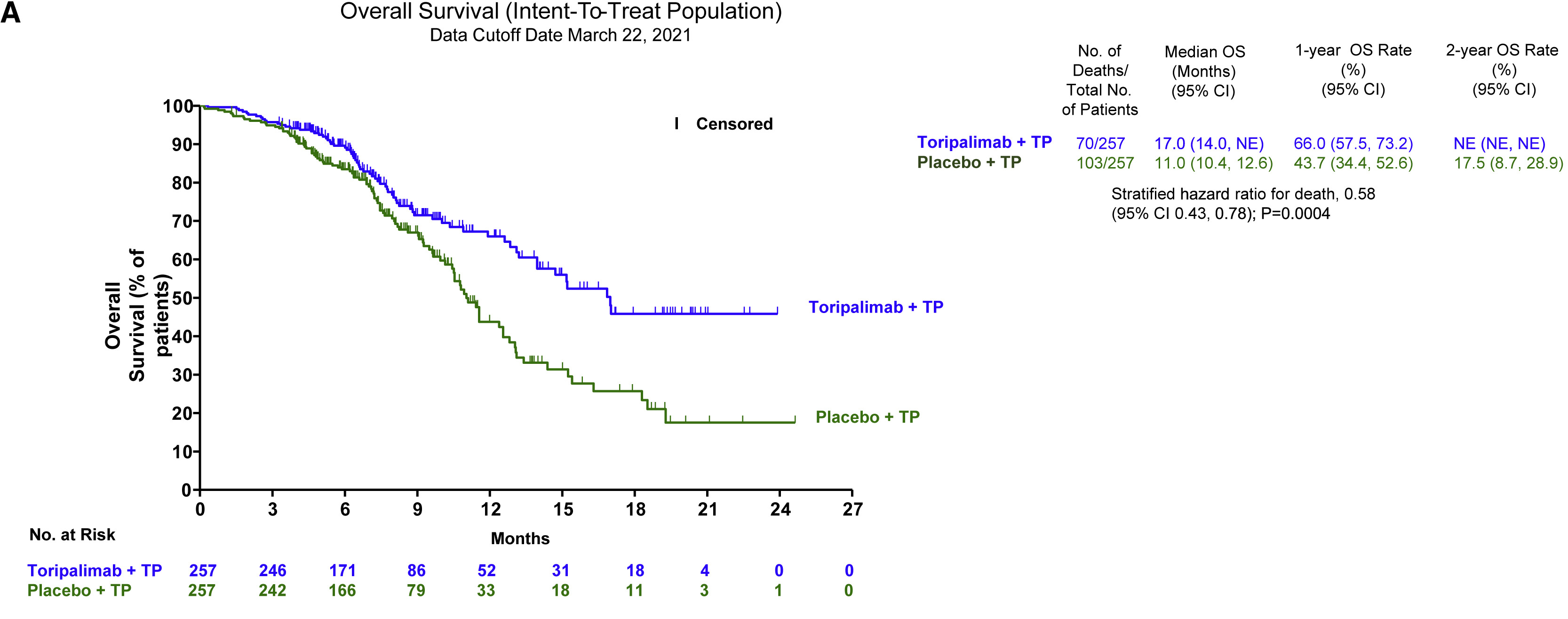
客观缓解率(ORR)分别为69.3%和52.1%,疾病控制率(DCR)分别为 89.1%和82.1%,中位缓解持续时间 (DoR)分别为5.6 个月和 4.2 个月。
该试验表明,特瑞普利单抗联合治疗方案可显著改善初治晚期食管鳞状细胞癌 (ESCC)患者的中位生存期。
参考资料
1.https://jamanetwork.com/journals/jama/fullarticle/2812324
2.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10685882/












