3月4日,百济神州宣布美国食品药品监督管理局(FDA)已批准百泽安®(替雷利珠单抗)联合含铂化疗用于肿瘤表达PD-L1(≥1)的不可切除或转移性食管鳞状细胞癌(ESCC)成人患者一线治疗。

此次批准是基于3期RATIONALE-306(NCT03783442)试验的结果。该试验旨在评估百泽安®联合含铂化疗用于不可切除、局部晚期复发或转移性食管鳞状细胞癌(ESCC)成人患者一线治疗的有效性和安全性。
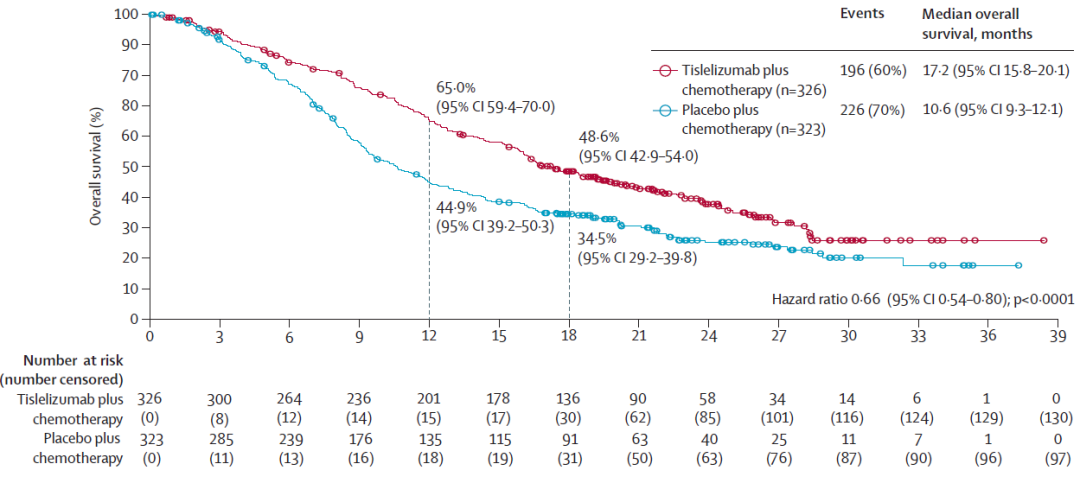
共649 例患者随机分配至替雷利珠单抗联合化疗组 (n=326) 或安慰剂联合化疗组 (n=323)。替雷利珠单抗组的中位总生存期为 17·2 个月,安慰剂组为 10·6 个月。替雷利珠单抗组中位无进展生存期(PFS)为7.3个月,安慰剂组为5.6个月,客观缓解率(ORR)分别为63.5% 和42.3%,中位持续缓解时间(DOR)分别为7.1个月和5.7个月。
百泽安(替雷利珠单抗)®是一款具有独特设计的人源化免疫球蛋白G4(IgG4)抗程序性细胞死亡蛋白-1(PD-1)单克隆抗体,能够以高亲和力和特异性与PD-1结合。其设计最大限度地减少与巨噬细胞中的Fcγ受体结合,帮助人体免疫细胞识别并杀伤肿瘤细胞。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.targetedonc.com/view/fda-approves-frontline-tislelizumab-plus-chemotherapy-in-advanced-escc

相关推荐
随便看看
- 地舒单抗注射液博洛加®在中国获批上市
- 阿美替尼肺癌辅助治疗适应症上市申请获受理
- ADC产品ADRX-0405完成临床首例受试者给药
- FDA 批准ribociclib联合芳香化酶抑制剂辅助治疗HR+/HER2- 早期乳腺癌患者
- 靶向CLDN18.2的ADC药物SHR-A1904治疗晚期胃癌或胃食管结合部癌(GC/GEJC)的研究数据登《Nature Medicine》
- APG-2449获国家药品监督管理局药品审评中心临床试验许可,用于非小细胞肺癌
- 德曲妥珠单抗6线治疗术后胃癌复发患者临床完全缓解
- 皮尔法伯实验室获得欧洲药品管理局人用药品委员会 (CHMP) 针对 BRAFTOVI®(康奈非尼)联合 MEKTOVI®(比美替尼)用于 BRAFV600E 突变晚期非小细胞肺癌 (NSCLC) 成人
- 帕妥珠单抗注射液上市申请获受理
- 昂阔医药ADC药物CUSP06初步1a期数据亮相2025 ASCO











