2月19日,勃林格殷格翰宣布美国食品药品监督管理局(FDA)已对其zongertinib (BI 1810631)的新药申请给予优先审评,用于治疗肿瘤具有HER2 (ERBB2)突变且既往接受过全身治疗的不可切除或转移性非小细胞肺癌(NSCLC)成人患者。

该申请基于Ib 期Beamion LUNG-1 试验的阳性结果。Beamion LUNG-1 (NCT04886804)是一项开放标签的 I 期剂量递增试验,包括剂量确认和扩展,zongertinib 作为单药治疗具有 HER2 (ERBB2) 改变的不可切除或转移性实体瘤患者。2024年ESMO亚洲大会(于12月6日至8日在新加坡举行)上公布了BEAMION LUNG-1试验 Ib期队列1的最新研究数据,评估zongertinib(BI 1810631)在治疗携带人表皮生长因子受体-2(HER2)突变阳性晚期非小细胞肺癌(NSCLC)经治患者中的疗效。
经中心审查确认,zongertinib(剂量为每日120毫克,单次服用,n=75例患者)展现出卓越疗效:客观缓解率(ORR)为71%,疾病控制率(DCR)高达93%。
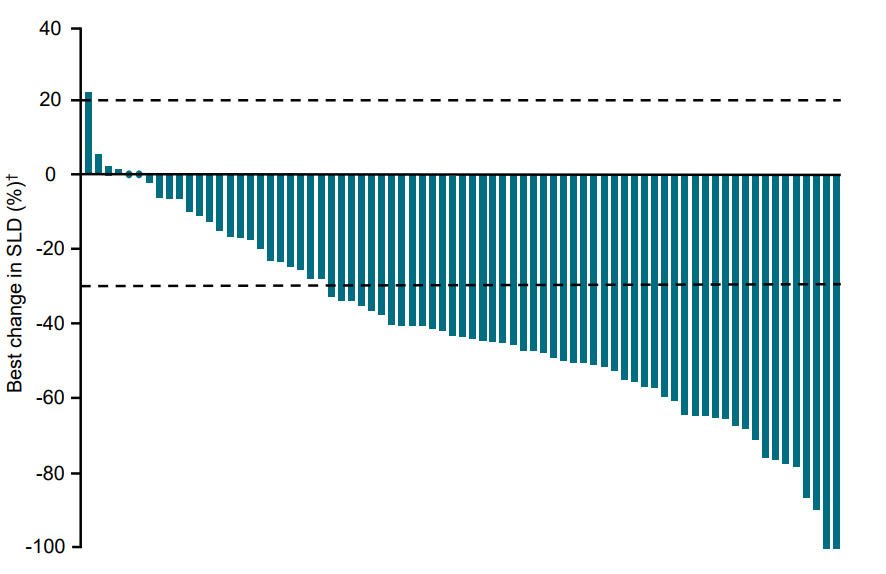
初步生存数据表明,zongertinib缓解持久:6个月无进展生存期(PFS)和缓解持续时间(DoR)比例分别为69%和73%。在数据截至时,仍有55%的患者仍在接受治疗。
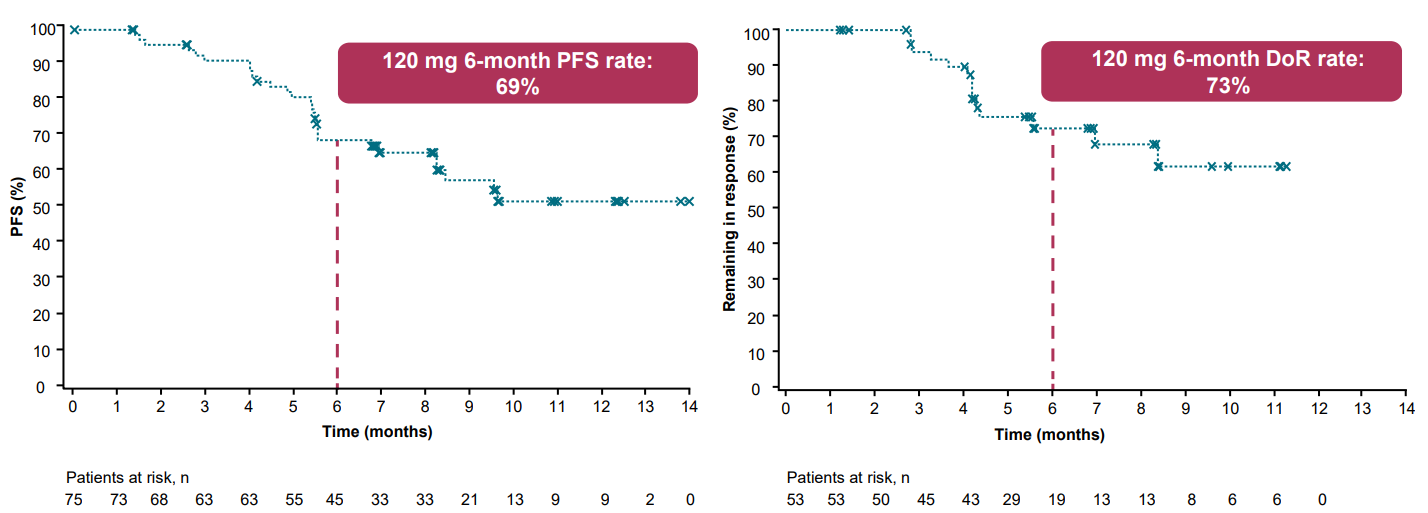
关于 zongertinib
Zongertinib (也称为 BI 1810631) 是一种在研的、不可逆的酪氨酸激酶抑制剂 (TKI),可选择性抑制 HER2 (ERBB2),同时保留 EGFR,从而限制相关毒性。这种口服靶向治疗正在开发用于 HER2 (ERRB2) 突变的晚期非小细胞肺癌 (NSCLC),并且 zongertinib 的其他临床研究正在具有 HER2 改变的实体瘤中进行。
目前有临床试验正在寻找肺癌患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
https://www.boehringer-ingelheim.com/human-health/cancer/lung-cancer/zongertinib-priority-review-fda-non-small-cell-lung-cancer

相关推荐
随便看看
- 疾病控制率高达92.4%!肺癌新款第三代EGFR抑制剂利厄替尼获得上市许可申请受理
- 西妥昔单抗N01注射液(达泰莱®)获批上市
- 转移病灶显著缩小!Selpercatinib获批新适应症,RET突变患者曙光
- 阿替利珠单抗
- 安尼妥单抗注射液拟纳入优先审评
- 即将上市!KRAS抑制剂Krazati联合疗法和D-1553优先审评
- 疾病控制率高达92.0%!赛沃替尼新适应症上市申请已获国家药监局受理
- SHR-A1921用于晚期小细胞肺癌(SCLC)的1期研究(NCT05154604)数据即将公布
- 诺诚健华多项研究数据亮相2025年第30届欧洲血液学协会(EHA)
- Ozuriftamab Vedotin获快速通道资格,用于治疗头颈鳞癌!











