2月7日,《Journal of Thoracic Oncology》发表了卡瑞利珠单抗联合立体定向放疗/全脑放疗(SRT/WBRT)及化疗用于既往未经系统治疗的驱动基因阴性、合并脑转移非小细胞肺癌(NSCLC)患者的CTONG2003研究数据。

CTONG2003研究是全球首个免疫联合放疗及化疗应用于晚期驱动基因阴性NSCLC脑转移患者的随机对照研究,该试验共纳入60例患者,其中32例分配至卡瑞利珠单抗组,28例分配至安慰剂组。
结果显示:卡瑞利珠单抗组颅内无进展生存期(iPFS)为12.7个月,安慰剂组为9.9个月,卡瑞利珠单抗组无进展生存期(PFS)为9.7个月,安慰剂组为6.7个月。
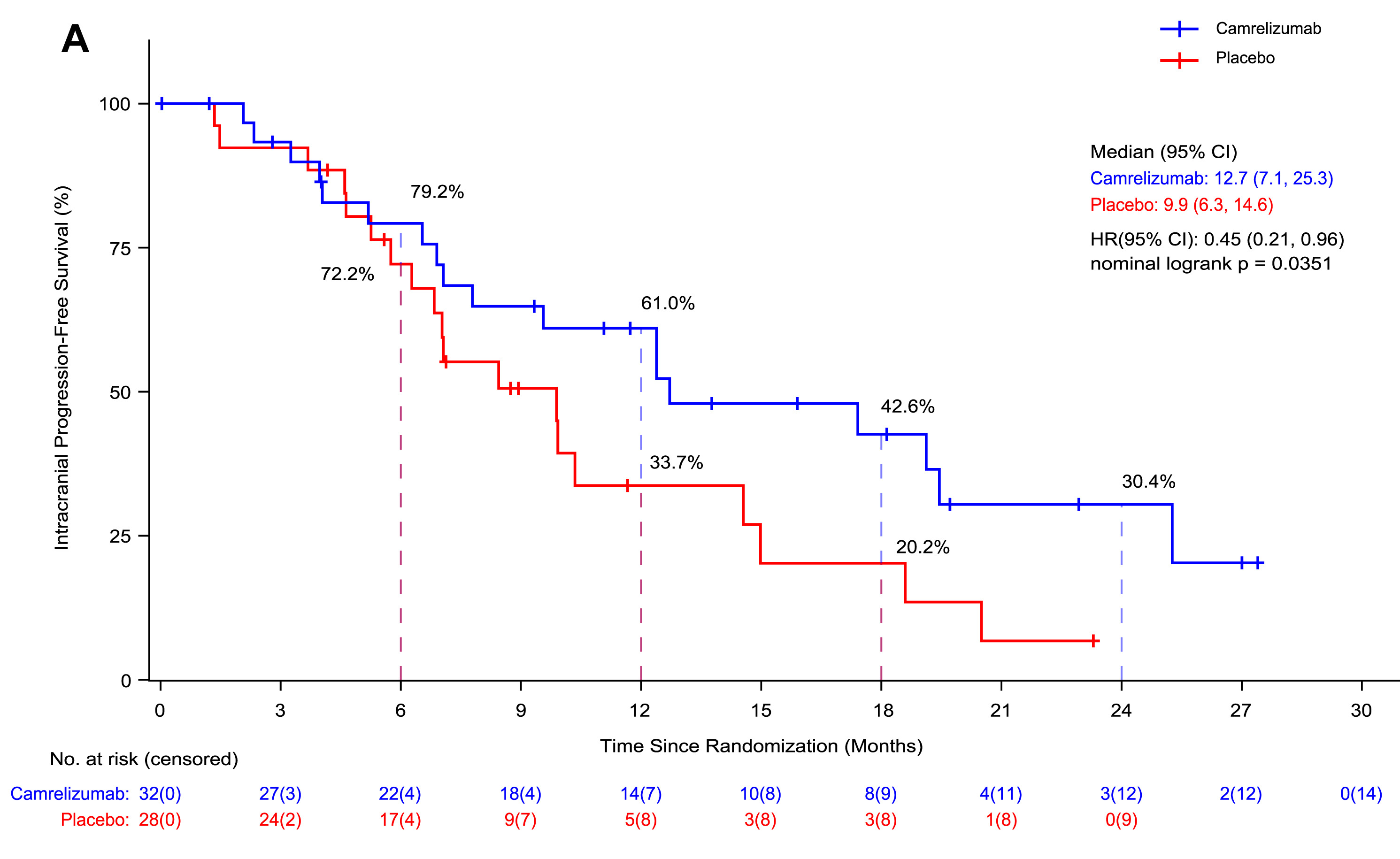
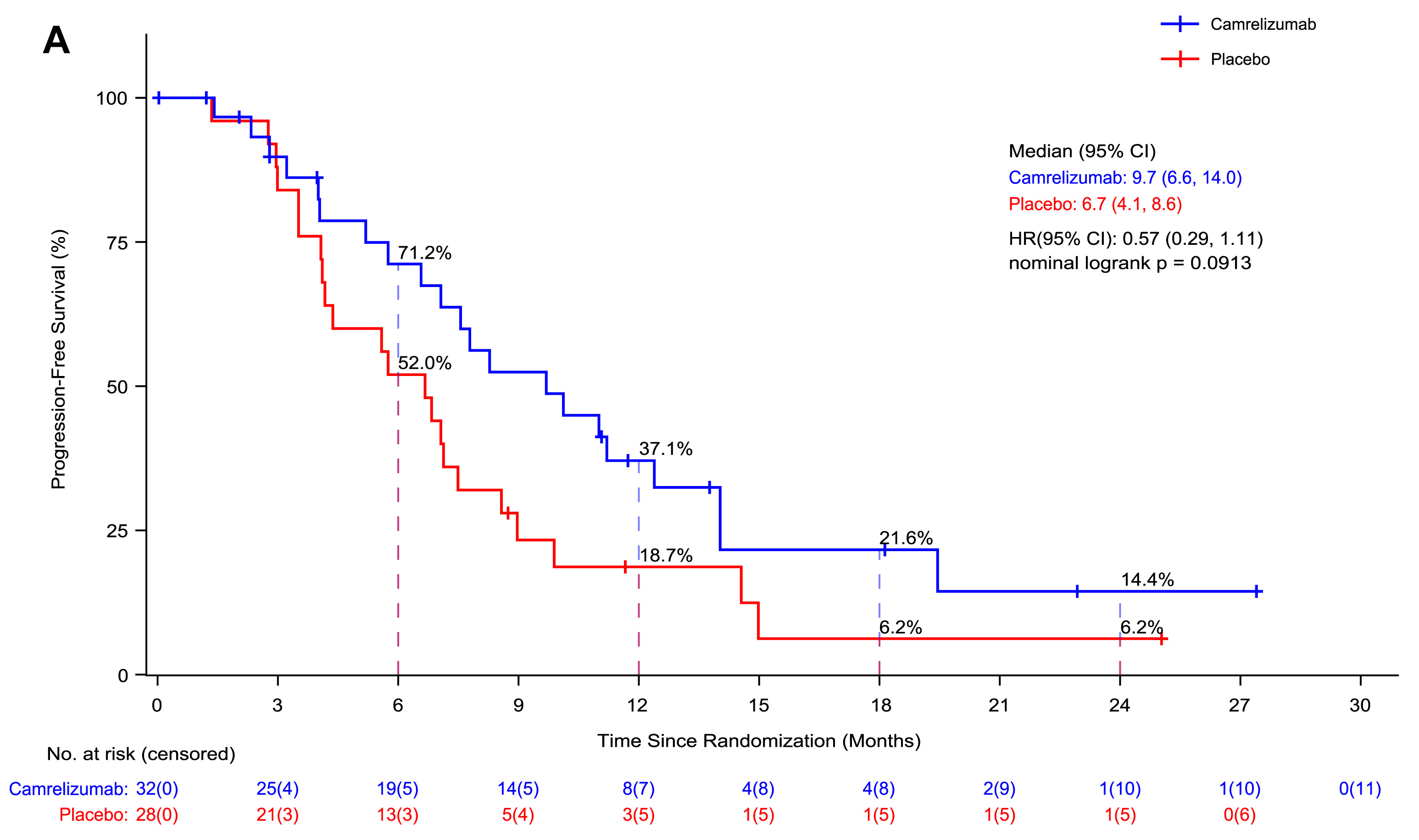
卡瑞利珠单抗组颅内客观缓解率(iORR)为 56.3%,2例患者完全缓解(CR),16例患者部分缓解(PR),12例患者病情稳定(SD)。卡瑞利珠单抗组的客观缓解率(ORR)为65.6%,安慰剂组为 32.1%。
安慰剂组颅内客观缓解率(iORR)为42.9%,1例患者完全缓解(CR),11例患者部分缓解(PR),12例患者病情稳定(SD)。
卡瑞利珠单抗组的中位颅内缓解持续时间(iDoR)为 16.3 个月,安慰剂组为 7.1 个月,卡瑞利珠单抗组的中位缓解持续时间(DOR)为 8.9 个月,安慰剂组为 4.2 个月。
卡瑞利珠单抗组的 12 个月 OS 率为 77.6%,安慰剂组为 60.7%。
卡瑞利珠单抗是一种单克隆抗体,作为程序性死亡受体1(PD-1)阻断剂,能结合T细胞表面的PD-1分子,并解除PD-1通路对T细胞的抑制作用。
卡瑞利珠单抗于2019年05月30日获NMPA批准上市,用于治疗:
1. 本品用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗。
2. 本品用于既往接受过索拉非尼治疗和/或含奥沙利铂系统化疗的晚期肝细胞癌患者的治疗。
3. 本品联合培美曲塞和卡铂适用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗。
4. 本品用于既往接受过一线化疗后疾病进展或不可耐受的局部晚期或转移性食管鳞癌患者的治疗。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.jto.org/article/S1556-0864(25)00063-2/fulltext

相关推荐
随便看看
- 宜联生物与安进达成合作协议,评估ADC药物YL201联合IMDELLTRA™用于广泛期小细胞肺癌的潜力
- 乘典生物CD-001获得国家药品监督管理局临床试验默示许可
- 疾病控制率达76.3%!新一代抗癌ADC药物:SKB264惊艳亮相
- KRAS G12C抑制剂MK-1084单药治疗及联合治疗的I期KANDLELIT-001研究登ASCO
- 中位生存期为21.4个月!Belzutifan亮相《新英格兰医学杂志》,肾癌患者新的治疗选择
- AK104注射液拟纳入突破性治疗
- 靶向CLDN18.2的ADC药物SHR-A1904治疗晚期胃癌或胃食管结合部癌(GC/GEJC)的研究数据登《Nature Medicine》
- 紫杉醇
- Dato-DXd在日本获批用于HR 阳性、HER2 阴性乳腺癌
- 客观缓解率为50%!特泊替尼的获批让携带MET外显子14 (METex14)跳跃的非小细胞肺癌治疗迎来新突破!











