近日,第56届美国妇科肿瘤学会(Society of Gynecologic Oncology,SGO)年会在美国西雅图举行。此次会议上报告了一项关于复发或转移性宫颈癌一线免疫联合治疗的随机对照III期研究(NCT05715840)的safety run-in数据。
该研究旨在评估恩朗苏拜单抗加含铂化疗联合/不联合贝伐珠单抗一线治疗PD-L1 阳性(CPS≥1)的复发或转移性宫颈癌的有效性和安全性。
16例患者接受恩朗苏拜单抗+化疗+贝伐珠单抗的联合治疗,15例患者接受恩朗苏拜单抗+化疗的联合治疗。结果显示:研究者评估的客观缓解率(ORR)为80.6%,其中5例患者完全缓解(CR),20例患者部分缓解(PR),3例患者病情稳定(SD),疾病控制率(DCR)为90.3%,中位缓解持续时间(DoR)未达到,12个月DoR率为51.6%,中位无进展生存期(PFS)为15.0个月。
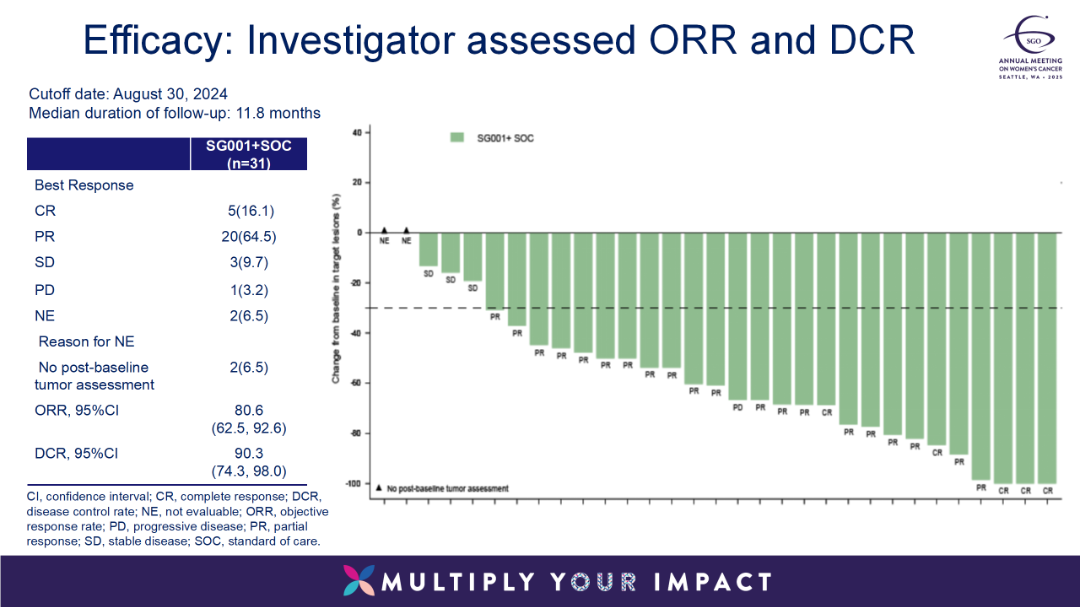
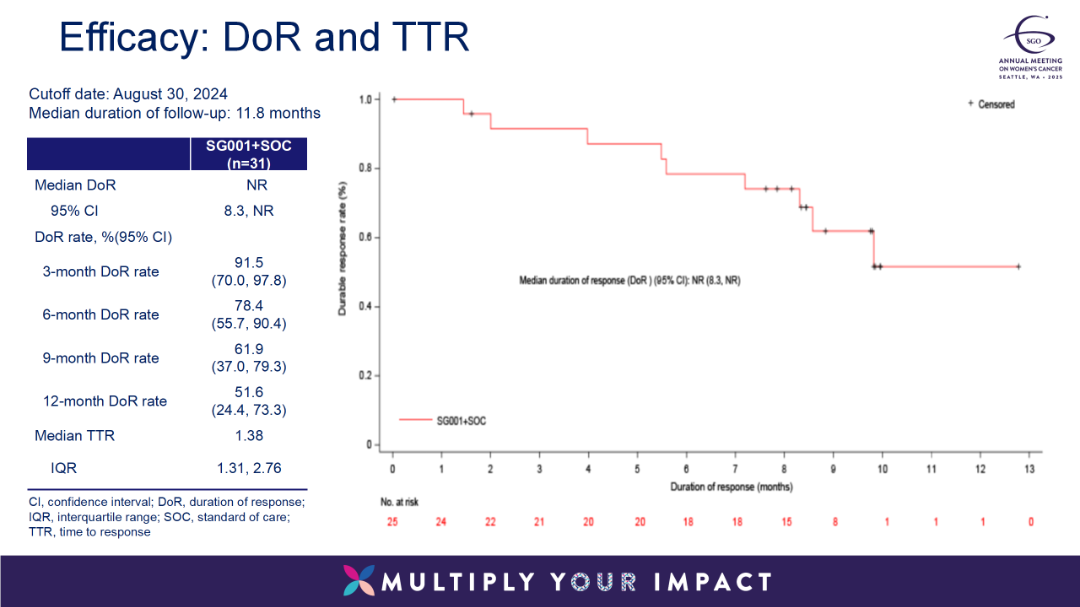
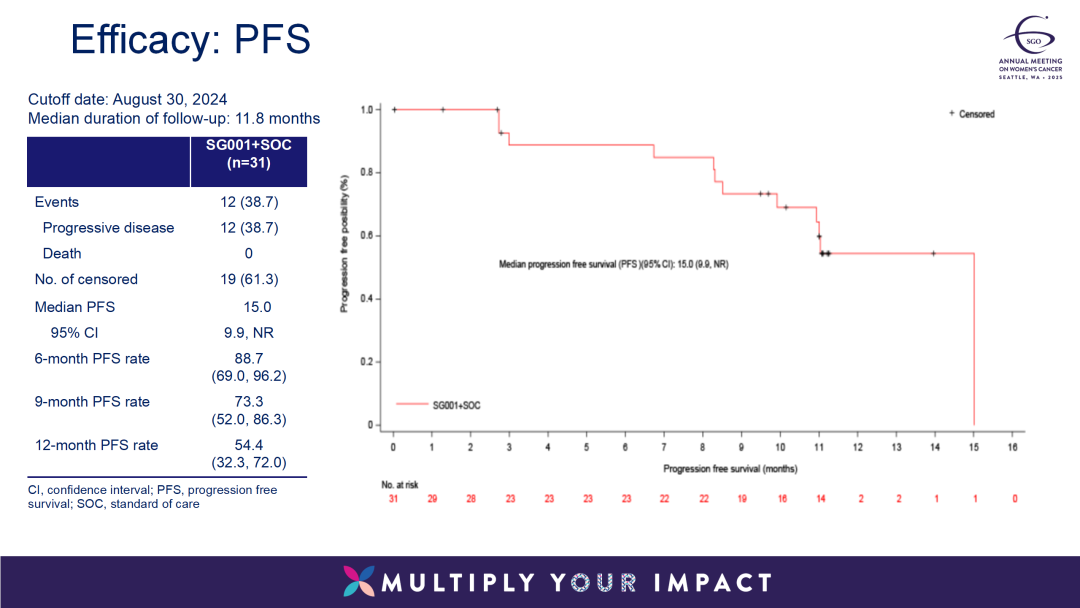
该试验表明,恩朗苏拜单抗+化疗+贝伐珠单抗的联合治疗方案一线治疗复发转移宫颈癌患者显示出有前景的疗效。
关于恩朗苏拜单抗
恩朗苏拜单抗(恩舒幸®)是 IgG4 亚型抗 PD-1 全人源单抗。可降低ADCC和CDC效应,通过与T细胞表面的PD-1分子结合,进而阻断PD-1/PD-L1通路对T细胞的抑制作用,使T细胞重新成为英勇的战士,显著发挥抗肿瘤作用。
2024年6月25日,恩朗苏拜单抗注射液(恩舒幸®)正式获得国家药品监督管理局的批准,用于既往接受含铂化疗治疗失败的PD-L1表达阳性(CPS≥1)的复发或转移性宫颈癌患者。
目前有临床试验正在寻找宫颈癌患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。

相关推荐
随便看看
- 格菲妥单抗新适应症获批,用于弥漫大B细胞淋巴瘤二线治疗
- 靶向CLDN18.2的ADC药物SHR-A1904治疗晚期胃癌或胃食管结合部癌(GC/GEJC)的研究数据登《Nature Medicine》
- ABSK-011胶囊拟纳入突破性治疗
- ADC药物BAT8006实现87.1%铂耐药卵巢癌(PROC)患者病情得到控制
- PD-1抑制剂帕博利珠单抗适应症扩展至PD-L1 CPS≥1的头颈部鳞状细胞癌患者
- “NTRK”跳出癌症包围圈,横跨多种癌种类型,为晚期癌症带来哪些全新的可能!
- 65岁患者用药1年后病灶几乎消失!西罗莫司为恶性血管周围上皮样细胞瘤带来3年生存希望,国内临床试验招募中
- PD-L1抑制剂度伐利尤单抗上市申请获得受理
- 全球首个且唯一高选择性JAK1抑制剂戈利昔替尼于国内首发上市!
- 欧盟委员会批准orspono用于治疗滤泡性淋巴瘤和弥漫性大B细胞淋巴瘤











