9月10日,国家药品监督管理局药品审评中心(CDE)显示:盛迪亚生物申报的注射用瑞康曲妥珠单抗拟纳入优先审评,用于治疗既往接受过一种或一种以上抗HER2药物治疗的局部晚期或转移性HER2阳性成人乳腺癌患者。

注射用瑞康曲妥珠单抗是恒瑞医药自主研发的、以HER2为靶点的抗体药物偶联物(ADC),可通过与HER2表达的肿瘤细胞结合并内吞,在肿瘤细胞溶酶体内通过蛋白酶剪切释放毒素,诱导细胞周期阻滞从而诱导肿瘤细胞凋亡。其释放的毒素具有高透膜性,可发挥旁观者杀伤效应,进一步提高抗肿瘤疗效。注射用瑞康曲妥珠单抗已于2025年5月获批上市,适应症为用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者,是国内首个获批用于HER2突变NSCLC患者的中国自主研发抗体偶联药物(ADC)。
2025年美国临床肿瘤学会(ASCO)年会上公布了瑞康曲妥珠单抗(SHR-A1811)在HER2阳性乳腺癌脑转移(BCBM)患者中的疗效与安全性。
REIN研究为一项双队列、多臂、Ⅱ期研究,纳入经病理确诊为HER2阳性或HER2低表达的乳腺癌患者,其中队列A入组HER2阳性乳腺癌患者,包含三个治疗组:
Arm 1:瑞康曲妥珠单抗6.4 mg/kg,Q3W
Arm 2:瑞康曲妥珠单抗 4.8 mg/kg联合吡咯替尼320 mg/d,Q3W(进行中)
Arm 3:瑞康曲妥珠单抗 4.8 mg/kg联合贝伐珠单抗15 mg/kg,Q3W
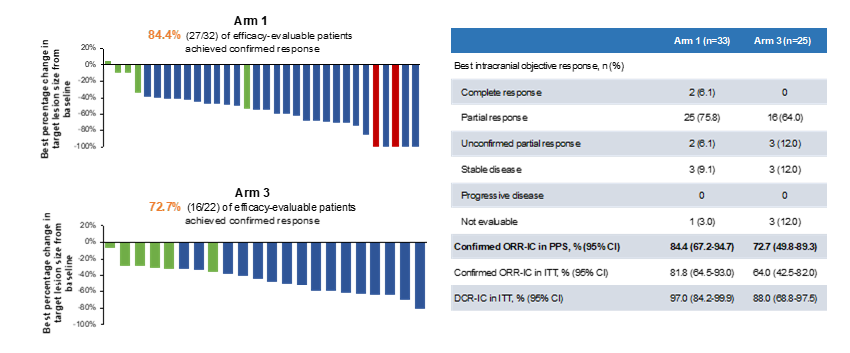
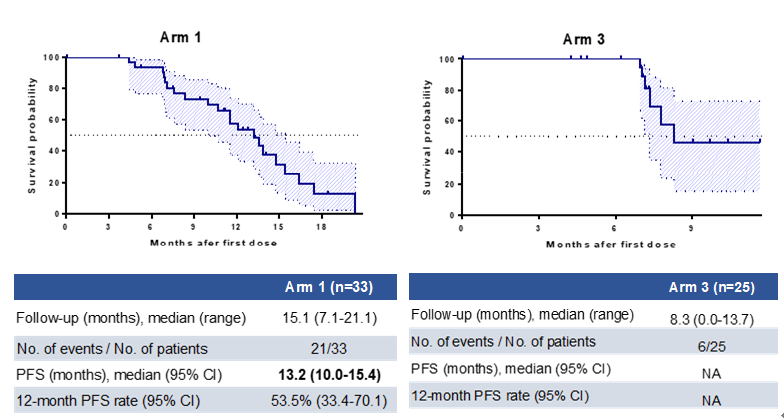
队列A中Arm 1(单药组)入组33例患者,Arm 3(联合组)入组25例患者,结果显示,单药组确认的ORR-IC为84.4%(27/32),其中2例(6.1%)达到完全缓解(CR),25例(75.8%)部分缓解(PR);颅内疾病控制率(DCR-IC)为97.0%,中位PFS为13.2个月,12个月PFS率为53.5%;联合组确认的ORR-IC为72.7%(16/22),DCR-IC为88.0%,中位PFS尚未成熟。两组治疗未观察到新的安全性信号。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找癌症患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 美国FDA授予EO-3021 快速通道资格,用于 Claudin (CLDN)18.2的胃癌/胃食管结合部癌症
- 宜联生物的注射用YL201拟纳入突破性品种,用于小细胞肺癌
- LM-108注射液拟纳入突破性治疗
- 注射用ZG006获得孤儿药资格认定
- 奥希替尼在日本获批新适应症
- 靶向FRα的ADC药物(BAT8006)针对铂耐药卵巢癌的III期临床试验完成首例受试者入组
- 帕博利珠单抗联合方案获美国FDA批准用于HER2阳性胃癌患者
- ADC药物-YL201让晚期实体瘤患者“柳暗花明”,在多种癌症治疗中大放异彩
- 普灵生物 ADC药物PLB-002临床试验申请获得美国FDA批准
- EPKINLY联合治疗方案获得美国FDA批准用于滤泡性淋巴瘤











