作者:小编
更新时间:2025-09-22
点击数:
9月19日,美国食品药品监督管理局(FDA)批准帕博利珠单抗和berahyaluronidase用于治疗成人和12岁及以上儿科患者中已获批使用帕博利珠单抗静脉注射剂型(商品名:Keytruda,默克公司)治疗的实体瘤适应症。

在MK-3475A-D77 (NCT05722015) 研究中评估了该联合治疗方案治疗转移性非小细胞肺癌患者的临床效果。共纳入377例患者被随机分配至帕博利珠单抗皮下联合化疗组(“帕博利珠单抗皮下注射组”,n = 251)或帕博利珠单抗静脉注射加化疗(“帕博利珠单抗静脉注射组”,n = 126)组,结果显示:帕博利珠单抗皮下注射组的ORR为45.4%,帕博利珠单抗静脉注射组的ORR为42.1%,帕博利珠单抗皮下注射组的中位 DOR 为 9.1 个月,帕博利珠单抗静脉注射组的中位 DOR 为 8.0 个月,帕博利珠单抗皮下注射组的中位PFS为8.1个月,帕博利珠单抗静脉注射组的中位PFS为7.8个月,帕博利珠单抗皮下注射组和帕博利珠单抗静脉注射组之间的 OS 事件发生率相当(24.3% vs 29.4%)。截至数据截止时,两个治疗组均未达到中位OS。
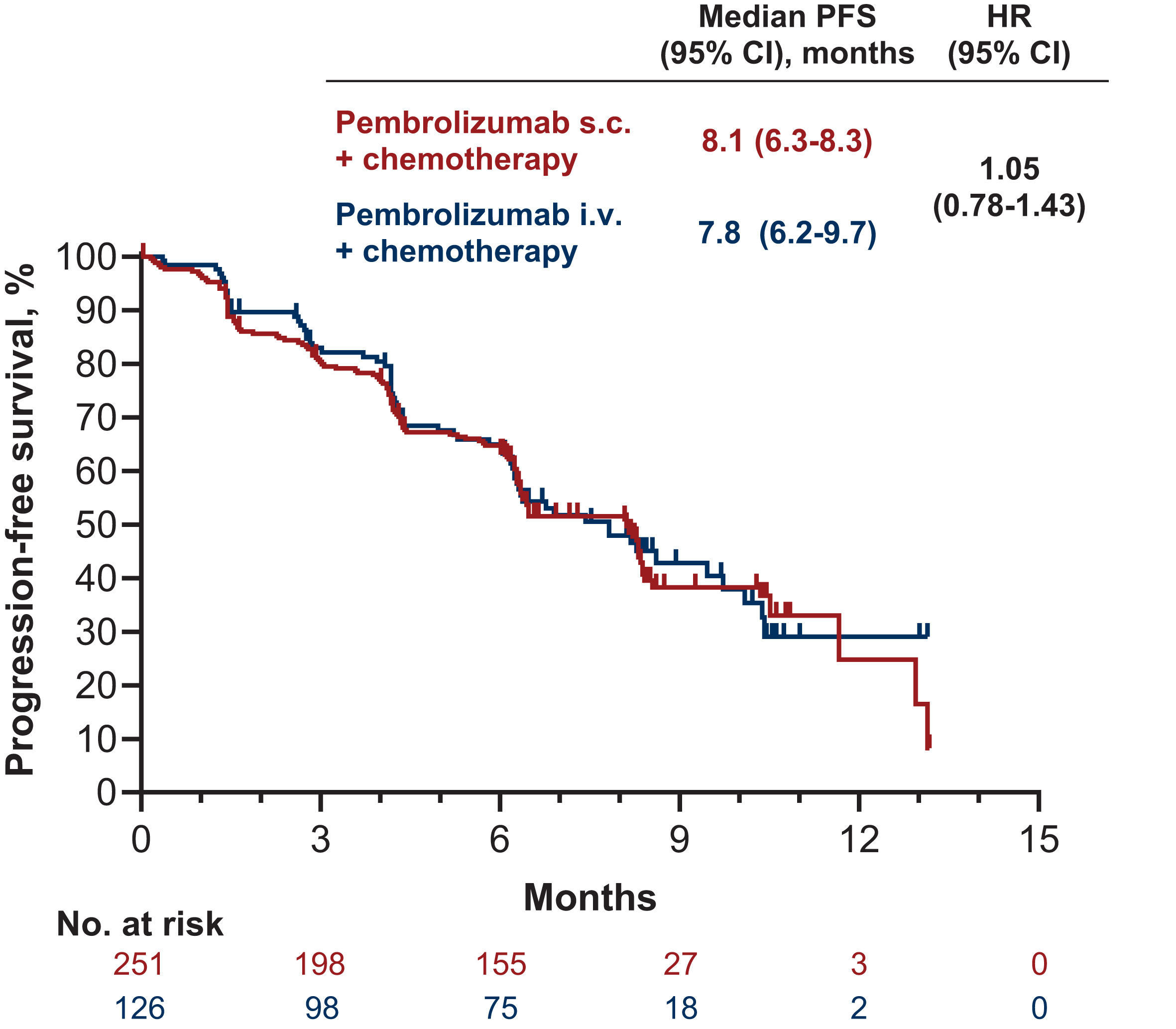
结果支持帕博利珠单抗皮下注射作为所有可使用帕博利珠单抗静脉注射的适应症的治疗选择。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。












