9月23日,科伦博泰的转染过程中重排(RET)小分子激酶抑制剂项目A400(亦称EP0031)的一项新药上市申请(NDA)已获中国国家药品监督管理局(NMPA)药品审评中心(CDE)受理,用于治疗RET融合阳性局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
A400是一款新型下一代选择性RET抑制剂,定位为治疗NSCLC、甲状腺髓样瘤(MTC)以及其他RET变异的高患病率实体瘤。
本次受理是基于KL400-I/II-01研究中两个关键2期队列治疗1L和2L及以上RET融合阳性NSCLC的积极结果。KL400-I/II-01研究中2期阶段包含队列1和队列2,分别评估A400/EP0031每天一次(QD) 90mg口服治疗经治和初治的RET融合阳性局部晚期或转移性NSCLC患者的有效性和安全性。
2023年美国临床肿瘤学会(ASCO)年会上报道了针对RET基因改变的晚期实体瘤患者的 I/II 期研究 (KL400-I/II-01, NCT05265091)。共纳入109例患者。60mg和90mg剂量组共纳入96例患者,其中69例为非小细胞肺癌(NSCLC),24例为甲状腺髓样癌(MTC)。90例患者疗效可评估确认的客观缓解率(ORR)为60%,疾病控制率(DCR)为94%。90mg剂量组,56例患者疗效可评估,ORR为63%,DCR为95%。
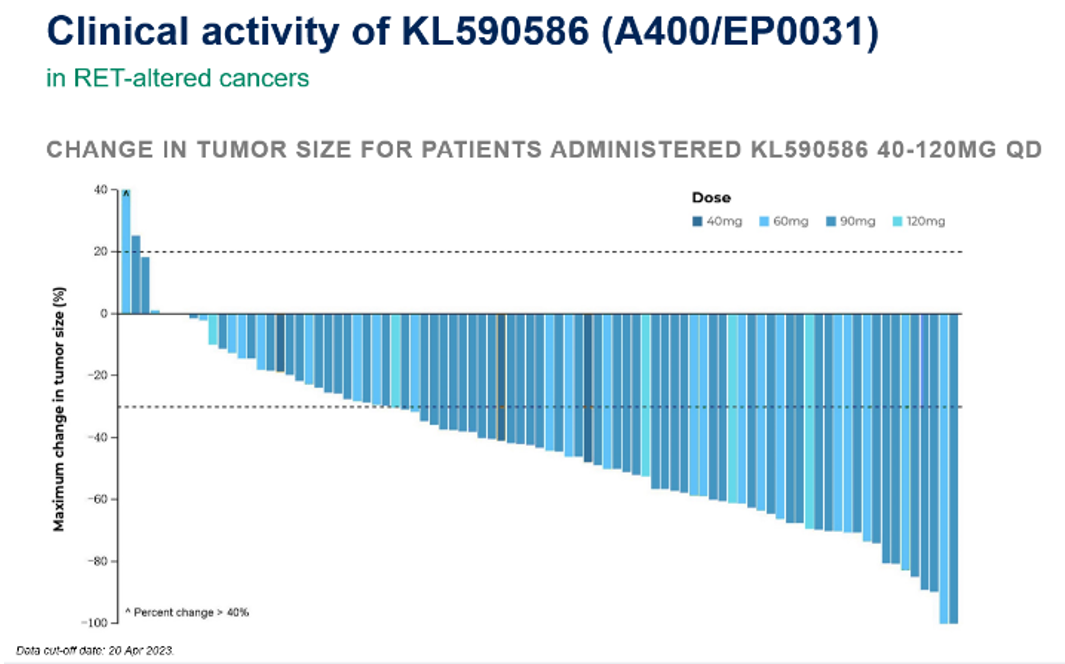
59例RET阳性NSCLC患者接受不同剂量A400治疗(40mg-120mg)且疗效可评估:
33例既往接受过系统治疗,在经治人群中A400的ORR达到69.7%,DCR为97%。26例既往未接受过系统治疗的患者,15.4%的患者基线存在脑转移,A400治疗一线人群的ORR可达80.8%,DCR为96.2%。

特别的是,A400在脑转移患者和经第一代SRI治疗后耐药的患者中,展现出初步的治疗潜力:
6例基线有可测量脑部病灶患者,5例患者脑部病灶缩小超过30%(5例均未接受过放疗),其中3例脑部病灶完全消失。

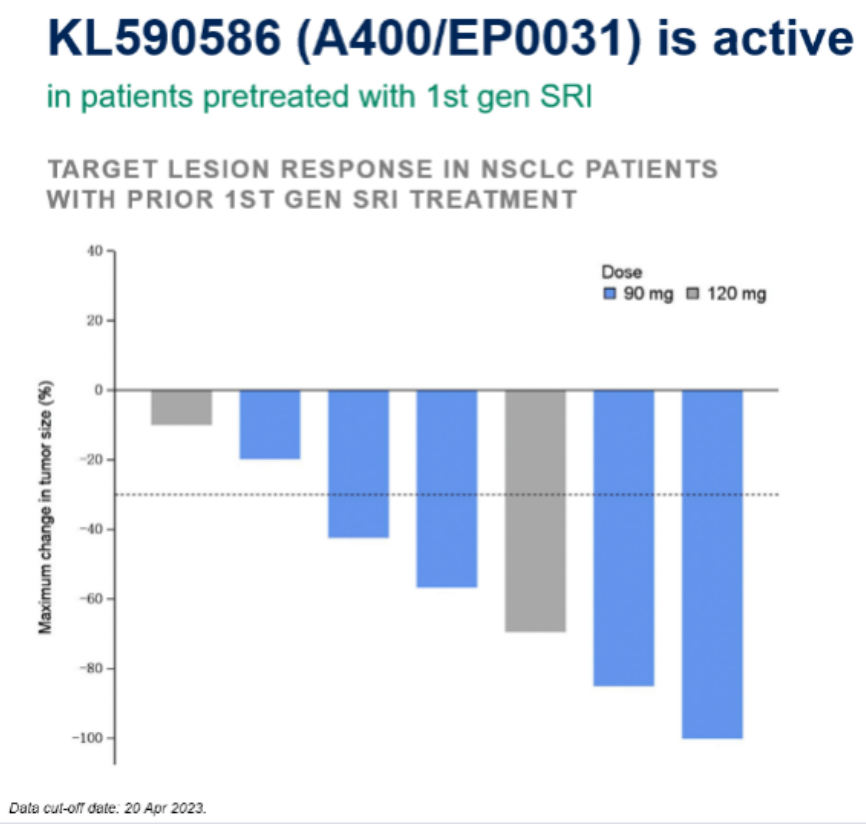
7例既往接受第一代SRI治疗后耐药的NSCLC患者,5例靶病灶缩小超过30%。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 胃癌患者新希望!德曲妥珠单抗国内申请新适应症,死亡风险直降30%
- 德达博妥单抗用于三阴性乳腺癌的TROPION-Breast02 Ⅲ期临床研究结果亮相2025 ESMO
- 2024年医保初审目录公示,ROS1/NTRK抑制剂瑞普替尼成功入选
- 瑞基奥仑赛注射液用于治疗系统性红斑狼疮患者的初步临床数据公布
- XNW27011拟纳入突破性治疗
- 利厄替尼片获批上市,用于EGFR T790M 突变阳性非小细胞肺癌
- 晚期宫颈癌、胃癌患者迎来新选择!肿瘤药物卡度尼利单抗亮相《柳叶刀》
- 美国FDA批准康方生物的派安普利单抗上市
- 美国FDA批准达雷妥尤单抗方案用于治疗多发性骨髓瘤患者
- 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款











