9月3日,Caribou Biosciences宣布,美国食品药品监督管理局(FDA)授予CAR-T 细胞疗法 CB-010快速通道资格用于难治性系统性红斑狼疮(SLE)。

截图来源于参考资料1,侵权请联系删除
CB-010 是同种异体 CAR-T 细胞治疗的主要临床阶段候选产品,4月4日,美国食品药品监督管理局(FDA)批准 CB-010 的研究性新药 (IND) 申请,用于治疗狼疮性肾炎 (LN) 和肾外狼疮 (ERL)。
CB-010 是临床上第一个具有 PD-1 敲除功能的同种异体 CAR-T 细胞疗法,也是第一个在2L LBCL环境下进行评估的抗CD19 异基因CAR-T细胞疗法。美国FDA曾授予CB-010再生医学高级治疗(RMAT)和B-NHL孤儿药指定。
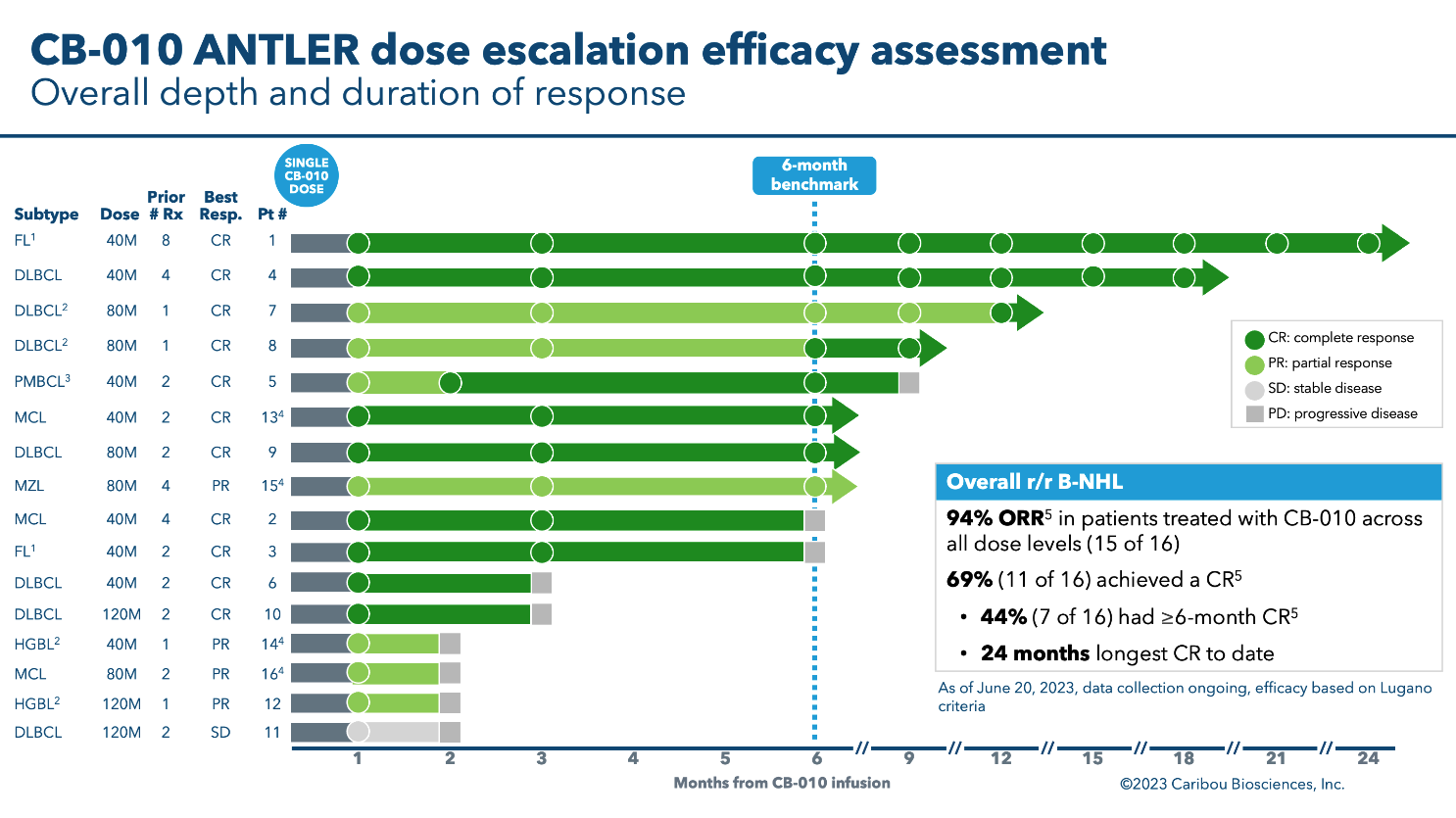
在I期ANTLER 试验中,评估了CB-010 在复发或难治性 B 细胞非霍奇金淋巴瘤 (r/r B-NHL) 患者中的疗效。结果显示:在16例患者中,总缓解率(ORR)高达94%,也就是说有15例患者出现了不同程度的缓解,其中11例患者实现完全缓解(CR),实现完全缓解的患者中,有7例患者最多在6个月时实现完全缓解,且持续完全缓解最长达到2年!
截图来源于参考资料2,侵权请联系删除
在10例大 B 细胞淋巴瘤 (LBCL)患者中,总缓解率(ORR)为90% ,其中有7例患者实现完全缓解,持续时间最长为1.5年!
该数据表明,CAR-T 细胞疗法 CB-010 在B 细胞非霍奇金淋巴瘤 患者治疗中具有显著疗效且耐受性良好。
此次CAR-T 细胞疗法 CB-010获得 快速通道资格用于难治性系统性红斑狼疮患者,将为系统性红斑狼疮患者带来新的治疗选择,期待临床试验能够取得不错的成绩。
目前康和源免疫之家有临床试验正在寻找系统性红斑狼疮患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
部分入选标准:
1.年龄≥18岁;
2.复发/难治性自身免疫性受试者,包括但不限于系统性红斑狼疮、特发性炎性肌病、系统性硬化症、干燥综合征、类风湿性关节炎、结缔组织病相关间质性肺病、免疫性血小板减少症、原发性胆汁胆管炎等。
3.预期生存时间≥3个月。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://investor.cariboubio.com/news-releases/news-release-details/caribou-biosciences-announces-fda-has-granted-fast-track
2.https://investor.cariboubio.com/news-releases/news-release-details/caribou-biosciences-reports-positive-clinical-data-dose

相关推荐
随便看看
- CAR-T产品倍诺达®(瑞基奥仑赛注射液)成功纳入首版国家医保局商业健康保险创新药品目录
- 多款CAR-T重拳出击!让更多淋巴瘤,胰腺癌,胃癌,肝癌等患者获益!
- CAR-T细胞产品(CT071)治疗多发性骨髓瘤实现100%缓解率
- 全球首个“纳米抗体装甲化”CAR-T临床研究结果公布
- 胰腺癌的新治疗:靶向药和CAR-T细胞来了
- 又一款CAR-T细胞疗法获批!B细胞急性淋巴细胞白血病患者获益
- 短短28天便改变了她的命运!《柳叶刀》重磅公布在研CAR-T细胞产品I期研究数据
- CAR-T细胞BTRP003H的研发成果亮相SITC2024
- 纳基奥仑赛注射液用于治疗自身免疫性溶血性贫血的新药临床试验申请获批
- 首个!12岁红斑狼疮女孩成功接受CAR-T治疗,有望彻底治愈!











