
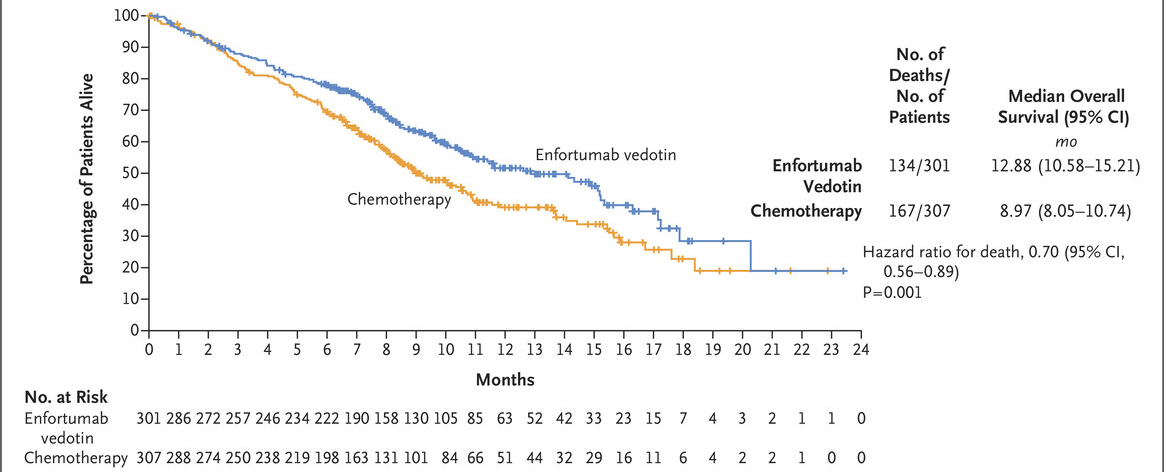
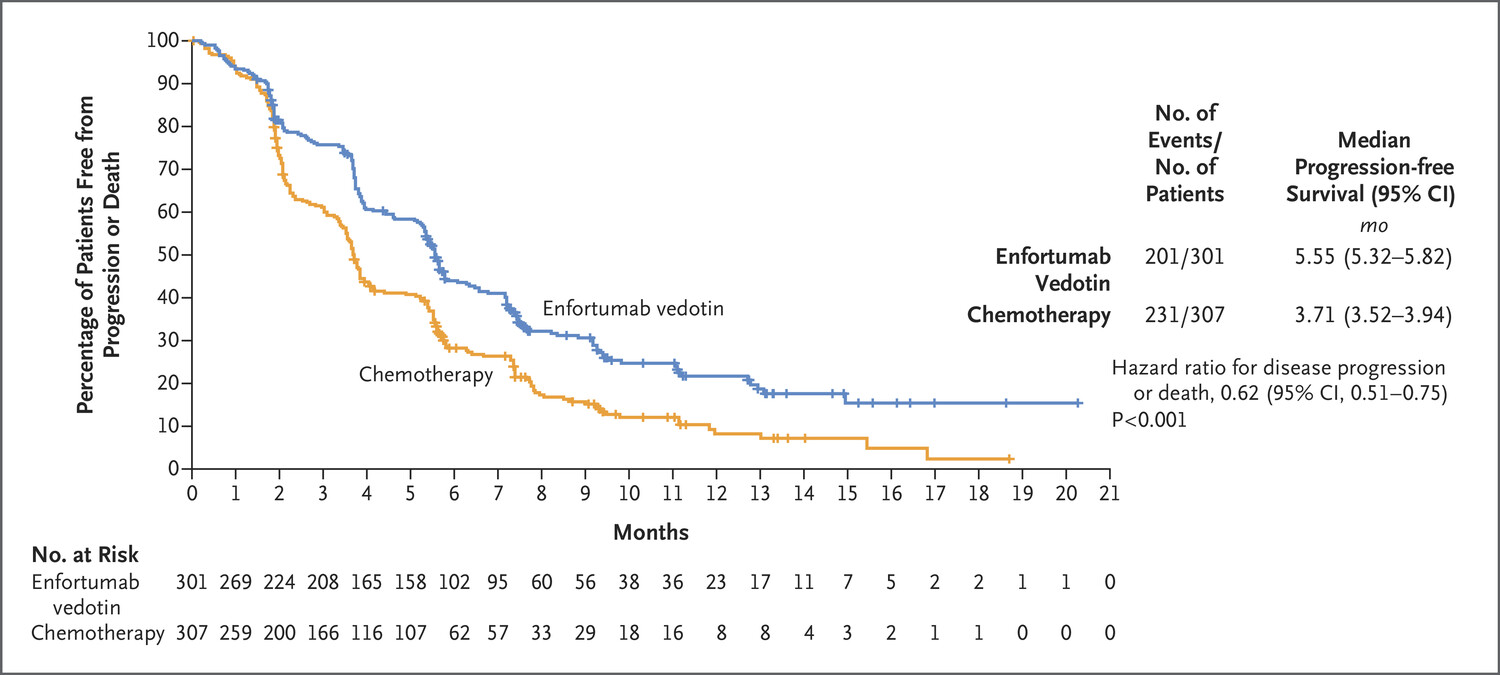
8月19日,国家药品监督管理局(NMPA)批准维恩妥尤单抗(备思复,PADCEV,enfortumab vedotin)用于治疗既往接受过含铂化疗和程序性死亡受体-1(PD-1)或程序性死亡配体 1(PD-L1) 抑制剂治疗的局部晚期或转移性尿路上皮癌(la/mUC)成年患者。 参考资料 1.https://www.prnewswire.com/news-releases/chinas-national-medical-products-administration-nmpa-approves-padcev-enfortumab-vedotin-for-treatment-of-locally-advanced-or-metastatic-urothelial-cancer-302225531.html 2.https://www.astellas.com/en/news/29366 3.https://www.nejm.org/doi/full/10.1056/NEJMoa2035807 4.https://ascopubs.org/doi/10.1200/JCO.2023.41.16_suppl.e16574 5.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.2545


相关推荐
随便看看
- BRAF V600E突变的非小细胞肺癌患者存活超14年!达拉非尼联合曲美替尼实现总生存期24个月
- 新型抗癌药物SYN818Ⅰ期临床试验启动会圆满召开
- 美国FDA批准礼来公司的塞普替尼(Retevmo)用于甲状腺髓样癌患者
- 多玛医药首个双抗ADC产品DM001正式获得美国FDA IND批准。
- Bcl-2抑制剂APG-2575联合阿扎胞苷治疗急性髓系白血病患者的最新数据公布
- HDP-101获批临床,拟用于治疗克隆性血液学疾病(如复发/难治性多发性骨髓瘤)
- 宜联生物与安进达成合作协议,评估ADC药物YL201联合IMDELLTRA™用于广泛期小细胞肺癌的潜力
- DCR达90.5%,IBI351 (KRAS G12C抑制剂)惠及肺癌、结肠癌患者
- 急性白血病新药Revumenib获得美国FDA批准上市
- ADC药物Blenrep联合方案获批用于多发性骨髓瘤











