9月20日,美国食品药品监督管理局(FDA)批准isatuximab-irfc(Sarclisa)联合硼替佐米、来那度胺和地塞米松用于治疗不符合自体干细胞移植(ASCT)条件的新诊断多发性骨髓瘤成人患者。

截图来源于FDA
关于 SARCLISA
SARCLISA (isatuximab-irfc) 是一种单克隆抗体,可与多发性骨髓瘤细胞上 CD38 受体上的特异性表位结合,诱导独特的抗肿瘤活性。它旨在通过多种作用机制发挥作用,包括程序性肿瘤细胞死亡(细胞凋亡)和免疫调节活性。
此次批准主要基于III期IMROZ(NCT03319667)试验,该试验数据于2024年6月发表于《新英格兰医学杂志》上。

截图来源于参考资料3,侵权请联系删除
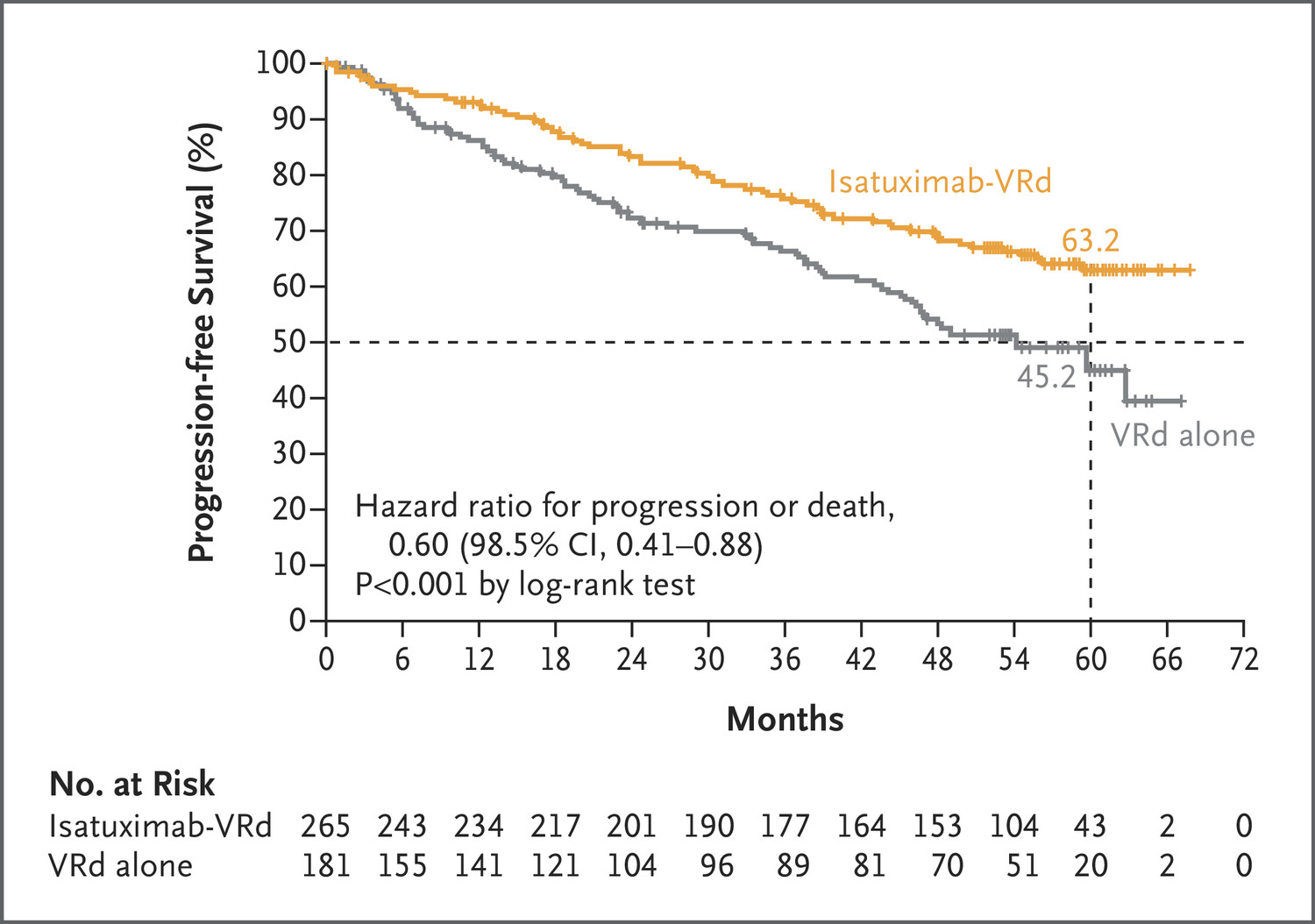
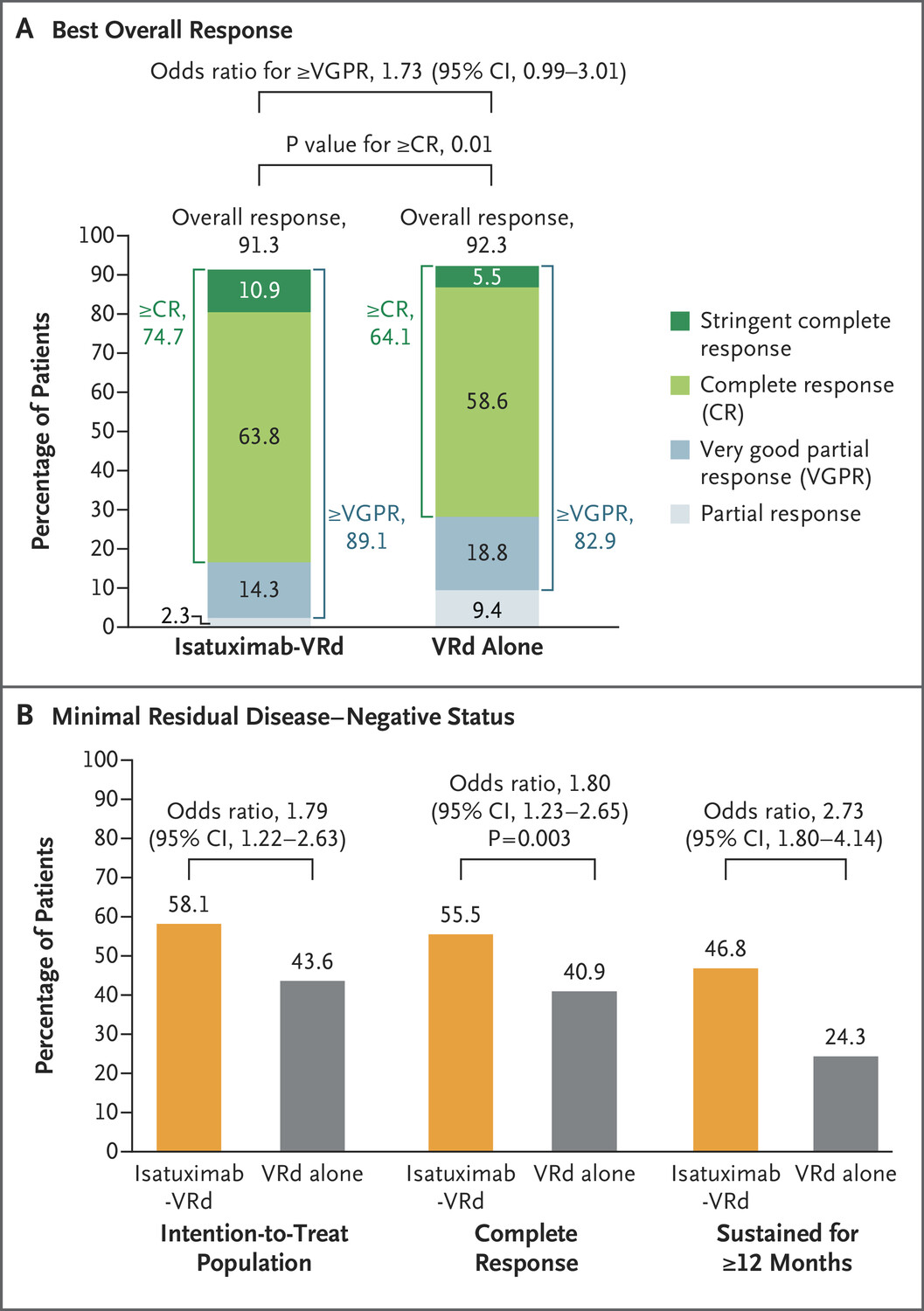
该试验共纳入446 例患者,其中265 例患者接受Sarclisa联合化疗治疗,181 例患者接受化疗,结果显示:联合治疗组总缓解率(ORR)为 91.3%,其中完全或更好缓解率为74.7%,无进展生存期(PFS)率为 63.2%,60 个月总生存率(OS)为 72.3%。
化疗组总缓解率(ORR)为92.3%,其中完全或更好缓解率为64.1%,无进展生存期(PFS)率为45.2%,60 个月总生存率为 66.3%。
截图来源于参考资料3,侵权请联系删除
联合治疗组有55.5%的患者微小残留病灶(MRD)状态有显著改善,有 46.8%的患者至少1年持续微小残留状态。化疗组有40.9%的患者微小残留病灶(MRD)状态有改善,24.3% 的患者至少1年持续微小残留状态。
截图来源于参考资料3,侵权请联系删除
该试验数据表明,对于不适合接受移植新诊断的多发性骨髓瘤患者,Sarclisa)联合硼替佐米、来那度胺和地塞米松比单纯化疗更有效。
目前康和源免疫之家有临床试验正在寻找多发性骨髓瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-isatuximab-irfc-bortezomib-lenalidomide-and-dexamethasone-newly-diagnosed-multiple
2.https://www.news.sanofi.us/2024-09-20-SARCLISA-R-approved-in-the-US-as-the-first-anti-CD38-therapy-in-combination-with-standard-of-care-treatment-for-adult-patients-with-newly-diagnosed-multiple-myeloma-not-eligible-for-transplant
3.https://www.nejm.org/doi/full/10.1056/NEJMoa2400712

相关推荐
随便看看
- 美国FDA批准ziftomenib用于NPM1 突变的复发或难治性急性髓性白血病患者
- 氟泽雷塞联合西妥昔单抗一线治疗KRAS G12C突变型非小细胞肺癌患者的II期研究最新疗效入选2025年欧洲肺癌大会
- 中位生存近5年!阿可替尼用于一线治疗慢性淋巴细胞白血病的新适应症获受理
- 注射用BL-M07D1拟纳入突破性治疗
- 美国FDA授予Dato-DXd突破性疗法认定
- 宗格替尼片(BI 1810631 片)拟纳入优先审评
- 吡托布鲁替尼(Pirtobrutinib)获得美国FDA批准用于慢性淋巴细胞白血病或小淋巴细胞淋巴瘤
- BRAF激酶抑制剂恩考芬尼上市申请获得受理
- 他泽司他联合 R-CHOP化疗方案治疗新诊断为弥漫性大 B 细胞淋巴瘤的老年患者的II 期EpiRCHOP研究结果公布
- 《临床肿瘤学杂志》发表了 FG-3246 在转移性去势抵抗性前列腺癌患者中的 1 期单药治疗研究结果











