10月9日,Can-Fite宣布,美国食品药品监督管理局(FDA)授予其肿瘤候选药物 Namodenoson(CF102)孤儿药资格认定,用于治疗胰腺癌。

Namodenoson是一种小型口服生物可利用药物,具有高亲和力和选择性结合肝癌和胰腺癌细胞表面的A3腺苷受体(A3AR)。
在Namodenoson治疗肝细胞癌的II期临床试验中,namodenoson 在评估人群中表现出良好的安全性和初步疗效信号。
该试验中共50例患者接受namodenoson治疗,28例患者接受安慰剂,结果显示:namodenoson 组的无进展生存期 (PFS) 为 2.5 个月,安慰剂组为 1.9 个月,namodenoson 组的中位 OS 为 4.1 个月,安慰剂组为 4.3 个月,1年生存率分别为 32% 和14%。

截图来源于参考资料2,侵权请联系删除
2024年4月,《《Experimental And Therapeutic Medicine》(《实验与治疗医学》)》报告了Namodenoson治疗晚期肝细胞癌的病例报告。

截图来源于参考资料3,侵权请联系删除
该患者于2016年11月28日参加Namodenoson治疗肝细胞癌治疗的研究试验,治疗前,患者肝脏有2个肿瘤病灶,肝脏右叶(VI 和 VII 段) 观察到较大的病灶,其最长直径为 91 mm。在右叶的 VI 段观察到较小的肝脏病变,其最长直径为 55 mm。此外,腹壁有2个病灶 (一个盆腔腹膜结节,最长直径为 20 mm,脐下腹膜结节最长直径为 18 mm),主动脉腔间淋巴结有另一个结节 (最长直径,16 mm)。基线时所有目标病灶的最长直径之和为 200 mm。此外,还注意到腹膜癌病。
2016 年 12 月 7 日开始接受Namodenoson治疗,大约 7 周后,肿瘤较小,实现部分缓解(PR),Namodenoson治疗 4 年的时间里,肿瘤、腹水和腹膜癌消失,实现完全缓解(CR)。
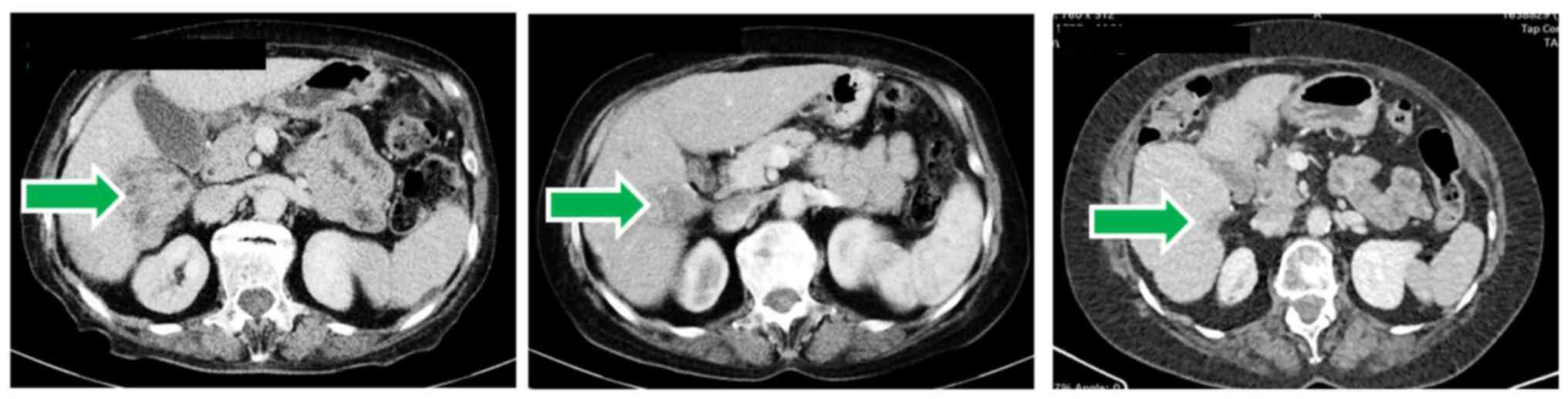
截图来源于参考资料3,侵权请联系删除
在Namodenoson治疗6年后,患者仍旧存活。
目前有临床试验正在寻找胰腺癌、肝细胞癌患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
2.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7825785/
3.https://www.spandidos-publications.com/10.3892/etm.2024.12551

相关推荐
随便看看
- 我国自主研发的EZH2抑制剂SHR2554在外周T细胞淋巴瘤中的关键临床研究结果亮相2025 EHA
- AUTX-703 被 FDA 授予复发或难治性急性髓性白血病快速通道资格
- 9MW2821获快速通道认定用于治疗局部晚期或转移性 Nectin-4 阳性三阴性乳腺癌
- 埃万妥单抗注射液一线治疗非小细胞肺癌正式在华上市
- 舒格利单抗获欧盟委员会批准用于一线治疗非小细胞肺癌
- 汇总|2023年国内上市的抗癌产品,重击骨髓瘤、白血病、肺癌、乳腺癌、肝癌等,肿瘤患者的福音
- 美国FDA批准imlunestrant用于ER+、HER2-、ESR1突变晚期乳腺癌
- 瑞基奥仑赛注射液用于治疗系统性红斑狼疮患者的初步临床数据公布
- 注射用HS-20093拟纳入突破性治疗,用于骨肉瘤
- 镥[177Lu]特昔维匹肽注射液纳入优先审评











