
10月8日,亚盛医药宣布国家药品监督管理局药品审评中心(CDE)批准APG-2449的临床试验申请,用于针对二代间变性淋巴瘤激酶(ALK)TKI耐药或不耐受的非小细胞肺癌(NSCLC)患者,或初治ALK阳性晚期或局部晚期非小细胞肺癌(NSCLC)患者的两项注册III期临床研究。
APG-2449是亚盛医药自主研发、具有口服活性的小分子FAK抑制剂,是ALK/ROS1多靶点抑制剂。


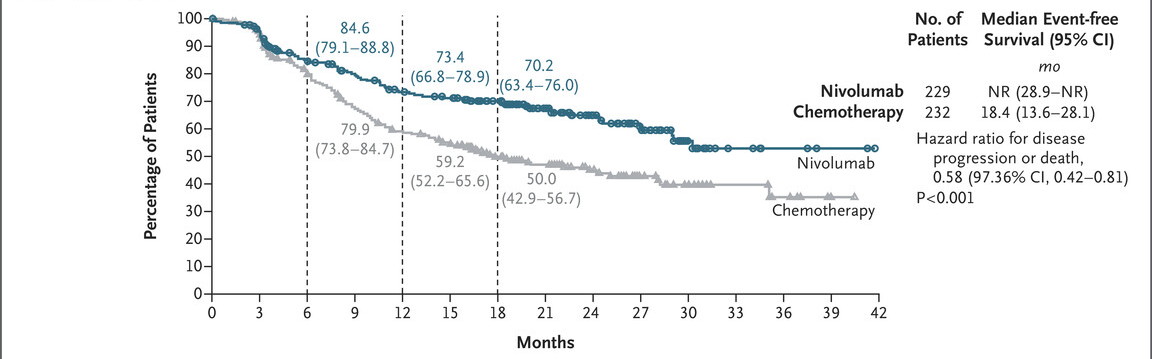
截图来源于参考资料2,侵权请联系删除 截图来源于参考资料3,侵权请联系删除 截图来源于参考资料3,侵权请联系删除 截图来源于ESMO 截图来源于参考资料5,侵权请联系删除 参考资料 1.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.3124 2.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-neoadjuvantadjuvant-nivolumab-resectable-non-small-cell-lung-cancer 3.https://www.nejm.org/doi/full/10.1056/NEJMoa2311926 4.https://www.annalsofoncology.org/article/S0923-7534(24)02836-9/fulltext 5.https://www.dizalpharma.com/news/detail?id=77&search=¤tPage=1




相关推荐
随便看看
- 美国FDA授予PYX-201 快速通道资格
- 第 40 届欧洲泌尿外科协会年会上报告了非肌层浸润性膀胱癌 (NMIBC) 患者 1 期试验的阳性数据
- 多玛医药首个双抗ADC产品DM001正式获得美国FDA IND批准。
- 注射用维贝柯妥塔单抗拟纳入优先审评
- 卡瑞利珠单抗联合放化疗治疗非小细胞肺癌脑转移患者临床研究登《Journal of Thoracic Oncology》
- FDA 扩大了 Pluvicto 的转移性去势抵抗性前列腺癌适应症
- 美国FDA授予注射用CBP-1019快速通道资格
- XNW5004片拟纳入突破性治疗
- 镥[177Lu]特昔维匹肽注射液纳入优先审评
- Sasanlimab的关键性III期CREST临床试验达到主要研究终点











