10月10日,美国食品药品监督管理局批准inavolisib(Itovebi)联合哌柏西利(palbociclib)和氟维司群(fulvestrant)用于治疗在接受辅助内分泌治疗后复发的内分泌耐药、PIK3CA 突变、激素受体 (HR) 阳性、人类表皮生长因子受体 2 (HER2) 阴性的局部晚期或转移性乳腺癌成人患者。

截图来源于参考资料1,侵权请联系删除
Inavolisib是一款口服、高选择性PI3Kα抑制剂,此次批准主要基于III期INAVO120 (NCT04191499)试验数据结果,该试验共纳入325例患者,结果显示:inavolisib组的客观缓解率(ORR)为58%,安慰剂组客观缓解率(ORR)为25%,中位缓解持续时间(DOR)分别为18.4个月和9.6个月。
inavolisib组的中位无进展生存期(PFS)为15.0个月,安慰剂组中位无进展生存期(PFS)为7.3个月。
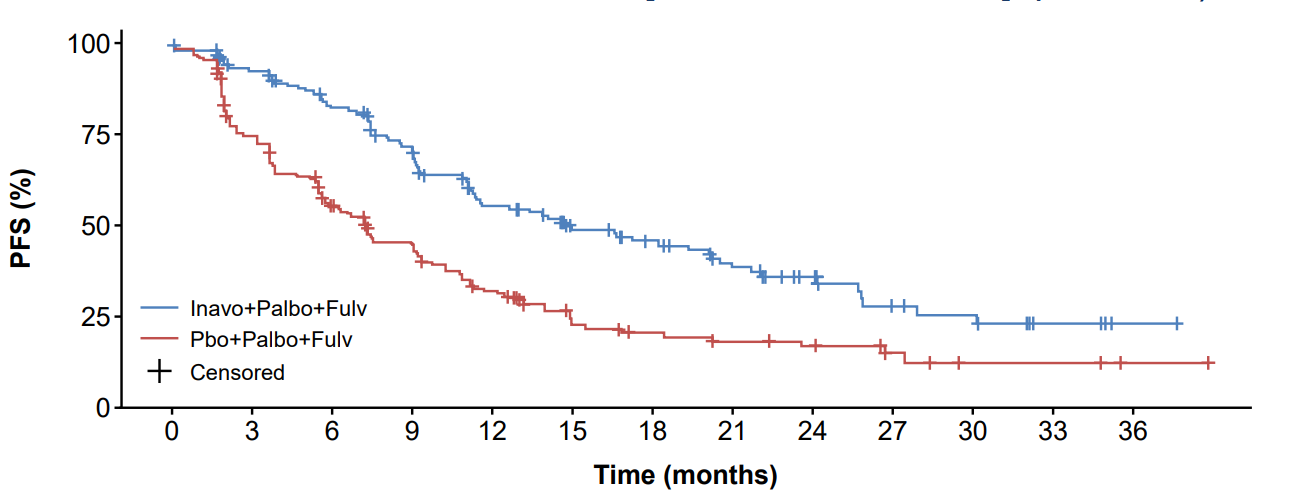
截图来源于参考资料2,侵权请联系删除
inavolisib组的6个月、12个月和18个月OS率分别为97.3%、85.9%和73.7%,而对照组分别为89.9%、74.9%和67.5%。
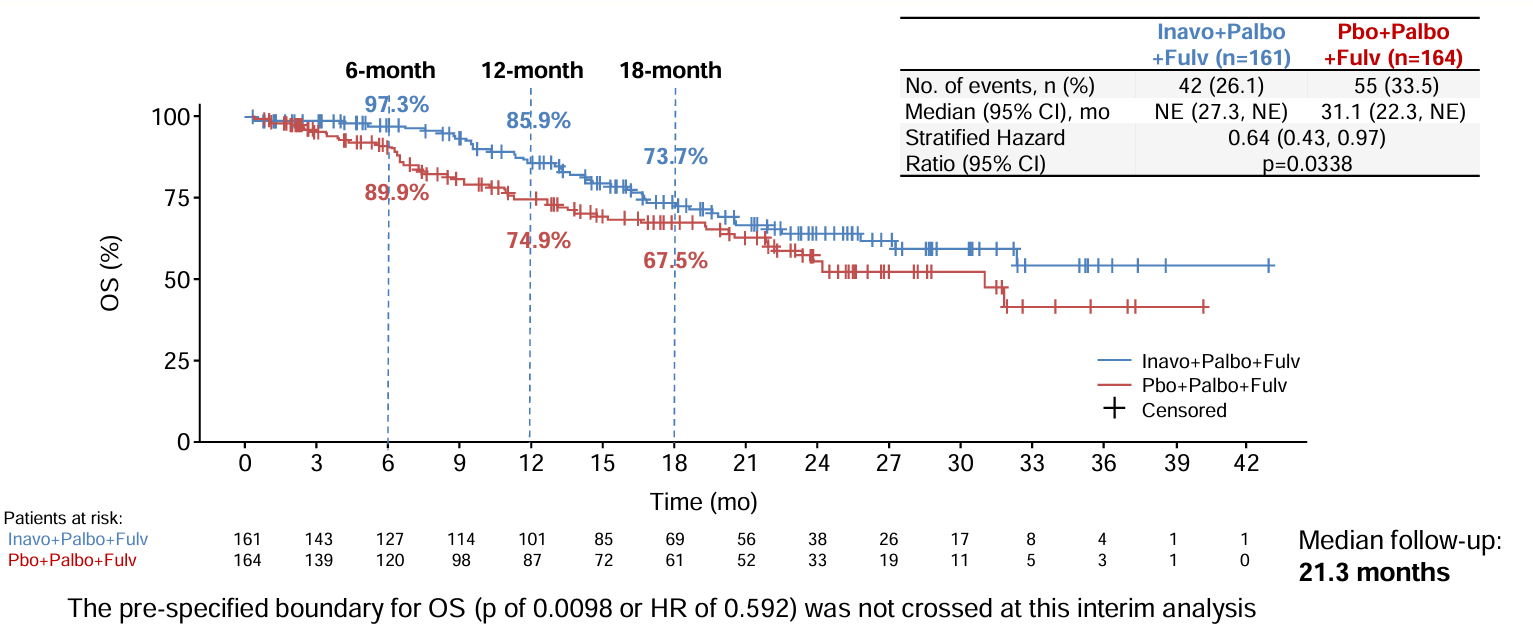
截图来源于参考资料2,侵权请联系删除
该试验中,与安慰剂相比,inavolisib组中位无进展生存期和缓解持续时间均得到显著延长。
乳腺癌患者如何寻找新的治疗方式
目前有临床试验正在全国范围内寻找乳腺癌患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-inavolisib-palbociclib-and-fulvestrant-endocrine-resistant-pik3ca-mutated-hr-positive
2.https://medically.roche.com/content/dam/pdmahub/restricted/oncology/annual-meeting-2024/oncology-annual-meeting-2024-presentation-juric-first-line-inavolisib-placebo-palbociclib.pdf

相关推荐
随便看看
- KRAS G12C抑制剂Krazati再获FDA批准,用于结直肠癌
- AK109注射液拟纳入突破性治疗
- 美国FDA批准拉泽替尼联合埃万妥单抗一线治疗EGFR 外显子19缺失或外显子21 L858R替换突变的非小细胞肺癌
- 新选择!奥希替尼联合化疗获批EGFR 突变晚期非小细胞肺癌!第四代靶向药带来更多治疗机会
- 5周脑转移灶完全消退!第四代ALK抑制剂NVL-655获美FDA突破性疗法认定!客观缓解率达71%!
- 全球首个!伯瑞替尼第三个适应症获批,用于单药治疗MET扩增非小细胞肺癌患者
- RET抑制剂A400/EP0031新药上市申请获受理
- 速看!Dato-DXd 在癌症治疗领域大放异彩,竟让癌症患者肿瘤“神奇消失”
- TIL疗法GC203治疗卵巢癌的最新临床研究结果
- 惊了!抗癌神药DS-8201终于在中国获批上市,生存期提高至10.1月











