12月31日,国家药品监督管理局(NMPA)批准安斯泰来申报的注射用佐妥昔单抗(商品名:威络益)上市。适应症为:联合含氟尿嘧啶类和铂类药物化疗用于CLDN18.2阳性、人表皮生长因子受体2(HER2)阴性的局部晚期不可切除或转移性胃或胃食管交界处(GEJ)腺癌患者的一线治疗。据了解,佐妥昔单抗是NMPA批准的首个靶向胃部肿瘤细胞表达生物标记物CLDN 18.2的单克隆抗体。

佐妥昔单抗是一种抗claudin 18剪接变体2(CLDN18.2)人鼠嵌合IgG1单克隆抗体,可特异性与CLDN18.2结合,诱导产生抗体依赖性细胞毒作用(ADCC)和补体依赖性细胞毒作用(CDC)。
GLOW及SPOTLIGHT两项III期临床研究的结果支持了NMPA的批准,GLOW研究评估了佐妥昔单抗联合CAPOX(一种包括卡培他滨和奥沙利铂的联合化疗方案)对比安慰剂联合CAPOX的疗效,POTLIGHT研究评估了佐妥昔单抗联合mFOLFOX6(一种包括奥沙利铂、亚叶酸和改良的5-氟尿嘧啶的联合化疗方案)对比安慰剂联合mFOLFOX6的疗效。9月16日,中山大学肿瘤防治中心徐瑞华教授在《新英格兰医学杂志》发表了Zolbetuximab(佐妥昔单抗)治疗胃或胃食管交界处腺癌((G/GEJ))患者的两项试验(SPOTLIGHT研究和GLOW研究)的综合分析。
共纳入1072例患者,其中537例患者接受Zolbetuximab组治疗,535例患者接受安慰剂组治疗,结果显示:Zolbetuximab组的中位无进展生存期(PFS)为9.2个月,安慰剂组为8.2个月,相比之下,疾病进展或死亡的风险降低了29%!
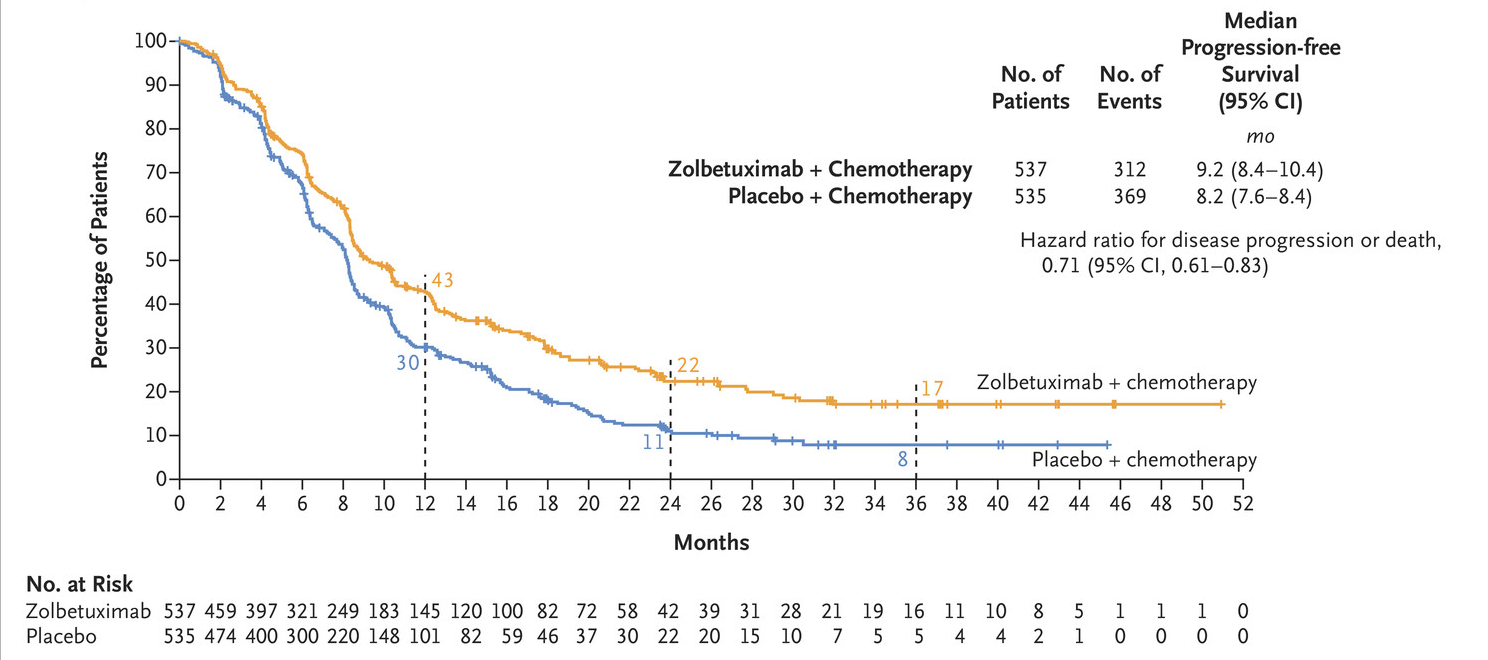
zolbetuximab组的中位总生存期(OS)为16.4个月,安慰剂组为13.7个月。
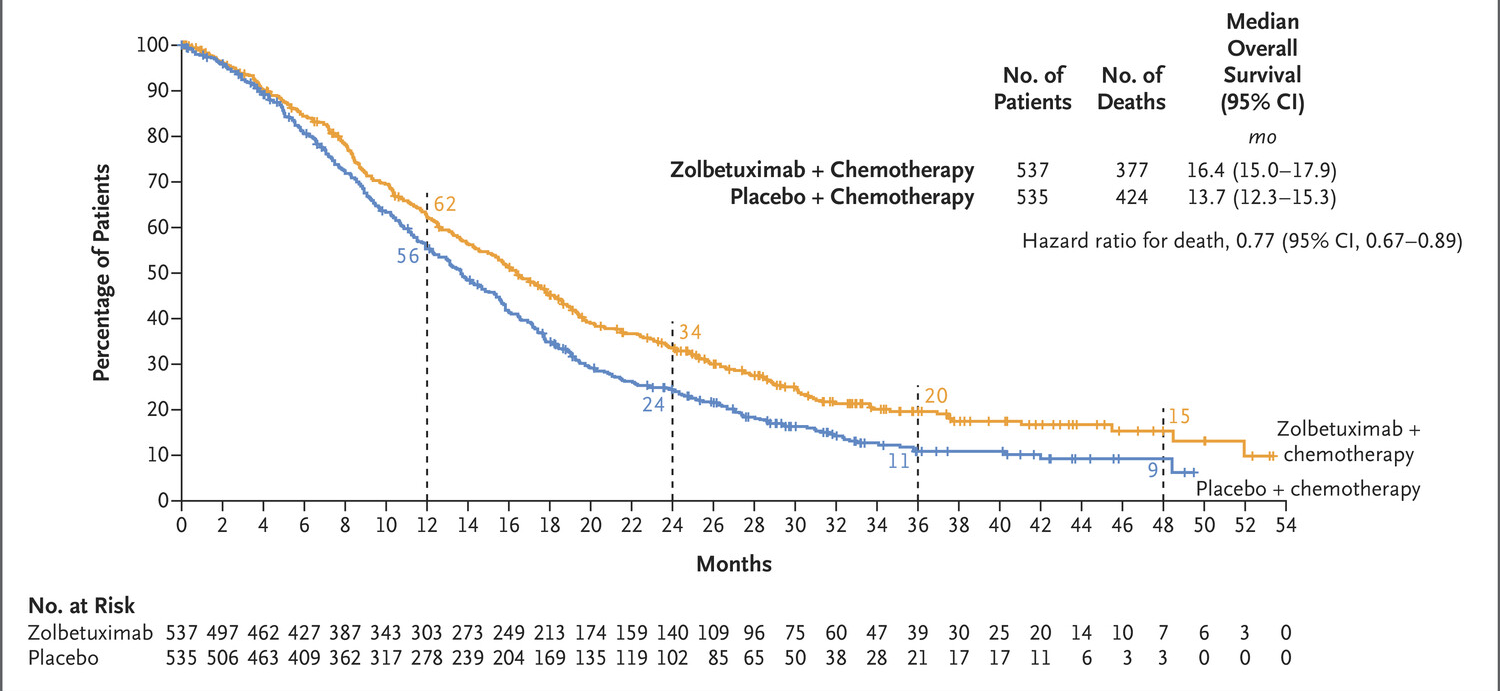
佐妥昔单抗的批准,为中国患者提供了新的一线精准治疗方案。
在 SPOTLIGHT 和 GLOW 研究中,佐妥昔单抗治疗组与对照组严重治疗中出现的不良事件(TEAEs)的发生率相似。佐妥昔单抗治疗组报告的最常见所有等级 TEAEs 包括恶心、呕吐和食欲减退。
胃癌是国内的高发癌种,2022年中国胃癌新发病例约35.9万,死亡病例约26.0万。
目前有临床试验正在寻找晚期或转移性胃/胃食管交界处腺癌患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
项目名称:一项评价注射用LM-302在CLDN18.2阳性的局部 晚期或转移性胃/胃食管交界处腺癌患者中有效性和安全性的随机、开放、多中心、阳性对照 III 期临床研究
部分入选标准:
1.年龄在18-80岁;
2.预计生存期≥12周;
3.局部晚期或转移性胃/胃食管交界处腺癌;
4.至少有1个可测量病灶;
5.美国东部肿瘤协作组(ECOG)评分为0~1分;
参考资料
https://www.nejm.org/doi/full/10.1056/NEJMc2409512?logout=true

相关推荐
随便看看
- 惊了!抗癌神药DS-8201终于在中国获批上市,生存期提高至10.1月
- ADC药物崭露头角,为肺癌、淋巴瘤、乳腺癌、胃癌患者打开生命新通道
- 芦康沙妥珠单抗新增适应症上市申请获受理
- GPRC5D CAR-T产品RD118新药临床试验申请(IND)获批
- 美国FDA批准retifanlimab联合方案用于肛管鳞状细胞癌
- ADC药物瑞康曲妥珠单抗(艾维达,SHR-A1811)上市
- IBI363获快速通道资格拟用于治疗黑色素瘤
- BRAF V600E突变的非小细胞肺癌患者存活超14年!达拉非尼联合曲美替尼实现总生存期24个月
- 德曲妥珠单抗治疗乳腺癌伴脑转移的病例报告
- 阿美替尼联合方案亮相2025 CSCO











