2025年1月17日,美国食品药品监督管理局(FDA)批准Datopotamab deruxtecan(Dato-DXd)用于不可切除或转移性激素受体(HR)阳性、人表皮生长因子受体 2 (HER2) 阴性(IHC 0、IHC1+ 或 IHC2+/ISH-)乳腺癌成人患者,这些患者既往接受过基于内分泌的治疗和化疗治疗不可切除或转移性疾病。

此次批准主要基于III期TROPION-Breast01试验结果,该试验评估了Dato-DXd 与研究者选择的化疗(ICC)在既往接受过治疗的不可切除或复发性 HR+/HER2– 乳腺癌患者中的疗效。2024年9月12日,《Journal of Clinical Oncology》发表了该试验结果。

该试验共360例患者纳入Dato-DXd组,351例纳入对照组,结果显示:Dato-DXd组有133例患者肿瘤缩小或消失,其中2例达到完全缓解(CR),131例达到部分缓解(PR),168例病情稳定(SD),中位缓解持续时间(DOR)为6.7个月,疾病控制率(DCR)为 75.3%。对照组84例患者肿瘤缩小或消失,均为部分缓解,176例患者病情稳定,疾病控制率为63.8%,中位缓解持续时间(DOR)为 5.7 个月。
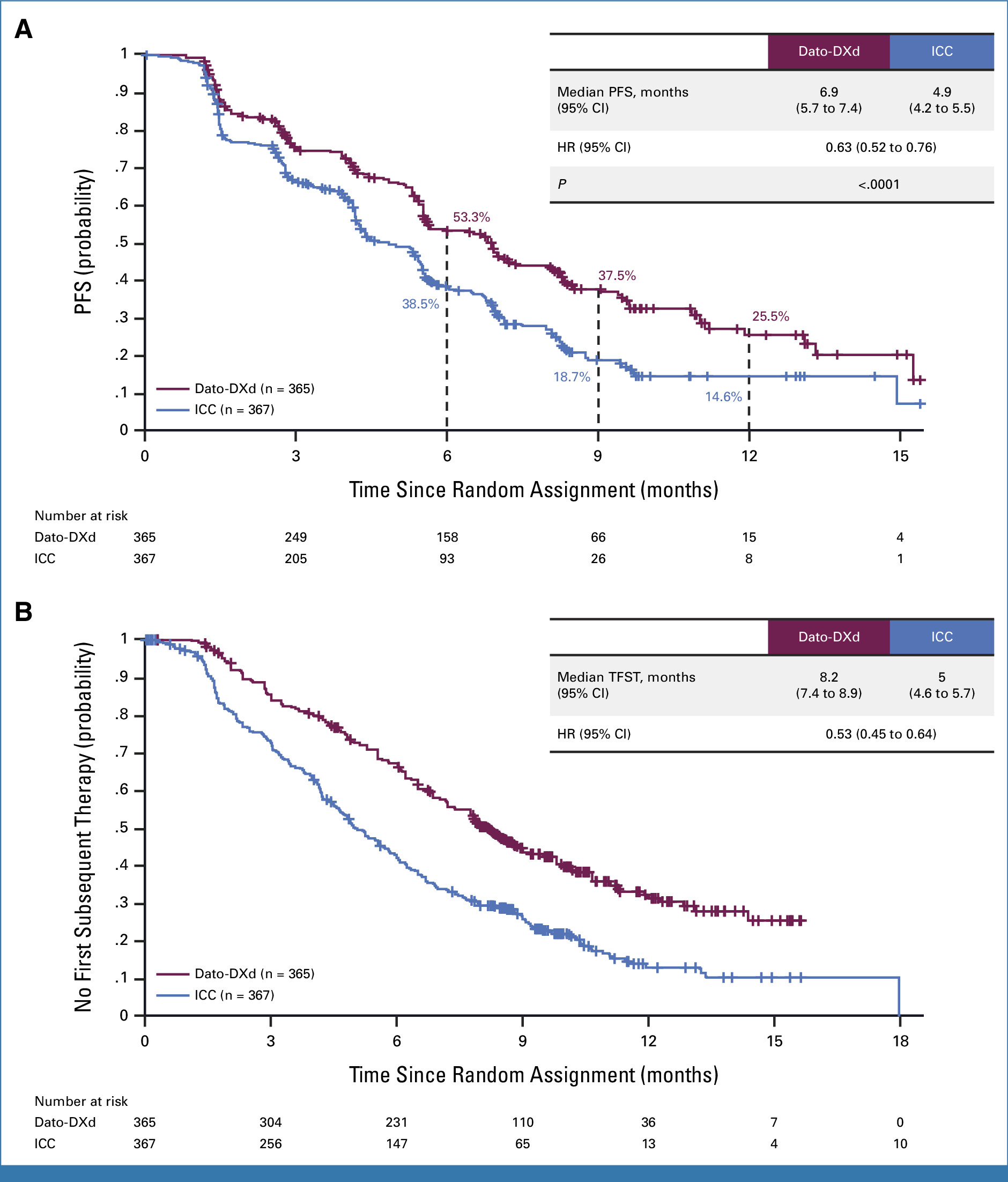
Dato-DXd组中位无进展生存期(PFS)6.9 个月,对照组为 4.9 个月,9 个月时,Dato-DXd 组有 37.5% 的患者无进展,而对照组组为 18.7%,在 12 个月时分别为 25.5% 和 14.6%。
目前ADC药物正在全国范围内寻找HER2过表达的实体瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以联系康和源免疫之家医学部(400-880-3716)。
部分入选标准:
1.年龄至少18岁;
2.晚期实体瘤患者;
3.ECOG体能状态评分为0~1。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-datopotamab-deruxtecan-dlnk-unresectable-or-metastatic-hr-positive-her2-negative-breast
2.https://ascopubs.org/doi/10.1200/JCO.24.00920

相关推荐
随便看看
- 两年缓解率接近100%!奥布替尼联合疗法一线治疗套细胞淋巴瘤全球三期临床启动
- 烨辉医药BN104片拟纳入突破性治疗
- Linvoseltamab治疗多发性骨髓瘤(MM)最新疗效数据公布
- Blenrep已获得欧盟批准,用于多发性骨髓瘤
- Tucatinib联合曲妥珠单抗治疗HER2突变转移性乳腺癌患者的2期SGNTUC-019试验公布
- 小细胞肺癌新药获批上市!无进展生存率提升近4倍!小细胞肺癌治疗的重大进步!
- 双特异性抗体Linvoseltamab治疗复发/难治性多发性骨髓瘤
- 正大天晴两款独家新药首次纳入医保目录
- 《临床肿瘤学杂志》上发表 Ziftomenib 在复发/难治性 NPM1 突变 AML 中的关键数据
- 总生存期17.3个月!美国FDA批准帕博利珠单抗联合培美曲塞和铂类化疗一线治疗恶性胸膜间皮瘤患者











