2月11日,美国食品药品监督管理局(FDA)批准brentuximab vedotin(Adcetris)与来那度胺和利妥昔单抗产品联合用于既往接受两线或以上全身治疗且不适合接受自体造血干细胞移植或CAR-T细胞治疗的复发或难治性大B细胞淋巴瘤(LBCL)成人患者。

此次获批主要基于3期ECHELON-3(NCT04404283)研究,在既往接受过2线或2线以上治疗且不适合干细胞移植(HSCT)或CAR-T治疗的复发/难治性或转化型DLBCL成人患者中,评估ADCETRIS联合来那度胺和利妥昔单抗联合安慰剂对比来那度胺和利妥昔单抗联合安慰剂的疗效。
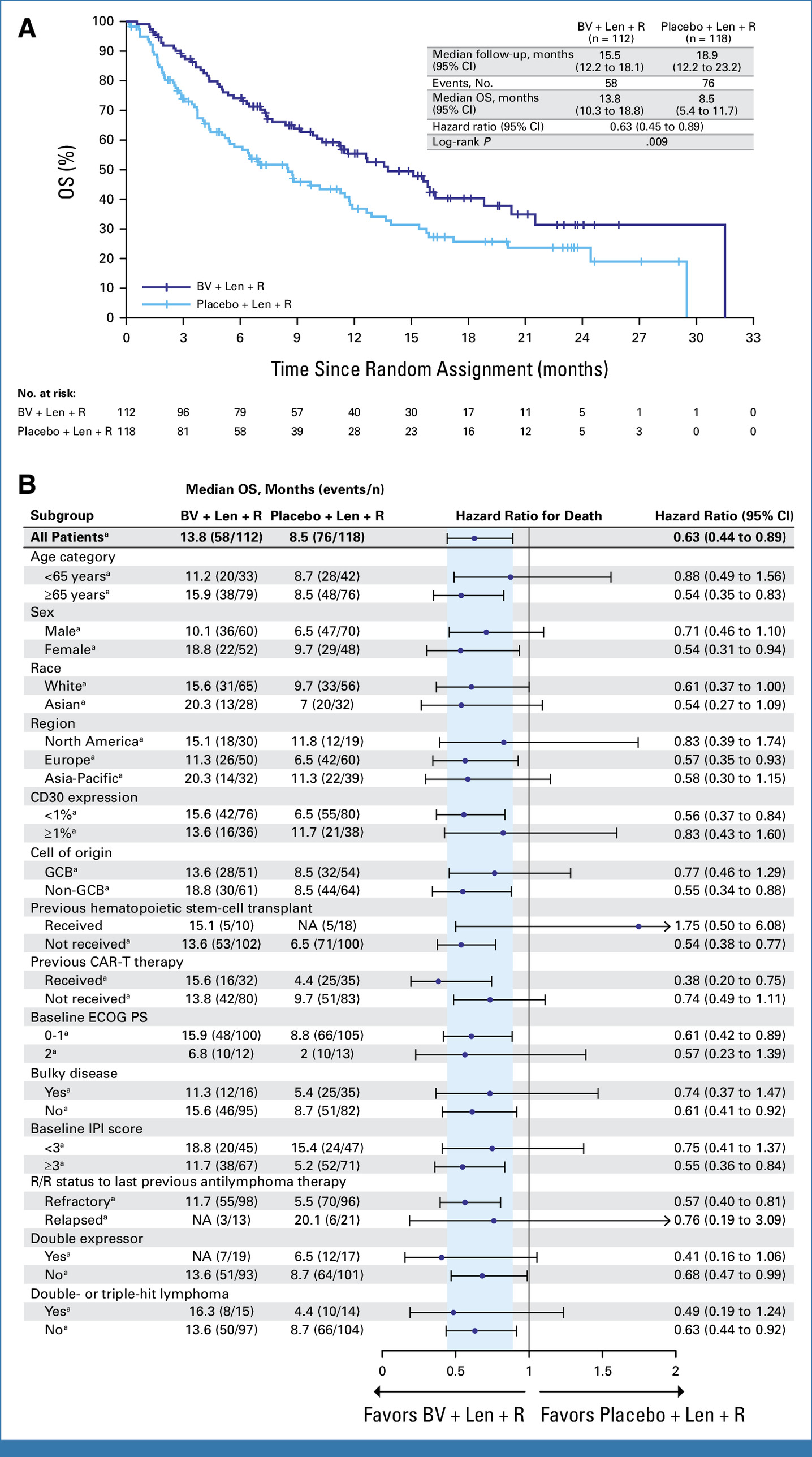
2025年1月7日,《JCO Oncology Practice》发布了ECHELON-3 的详细数据。共230例患者分别接受治疗,其中112名接受brentuximab vedotin与来那度胺和利妥昔单抗治疗,119名接受安慰剂联合来那度胺和利妥昔单抗治疗,结果显示:与安慰剂组相比,实验组死亡风险降低了 37%,中位总生存期(OS)分别为 13.8 个月 和 8.5 个月。
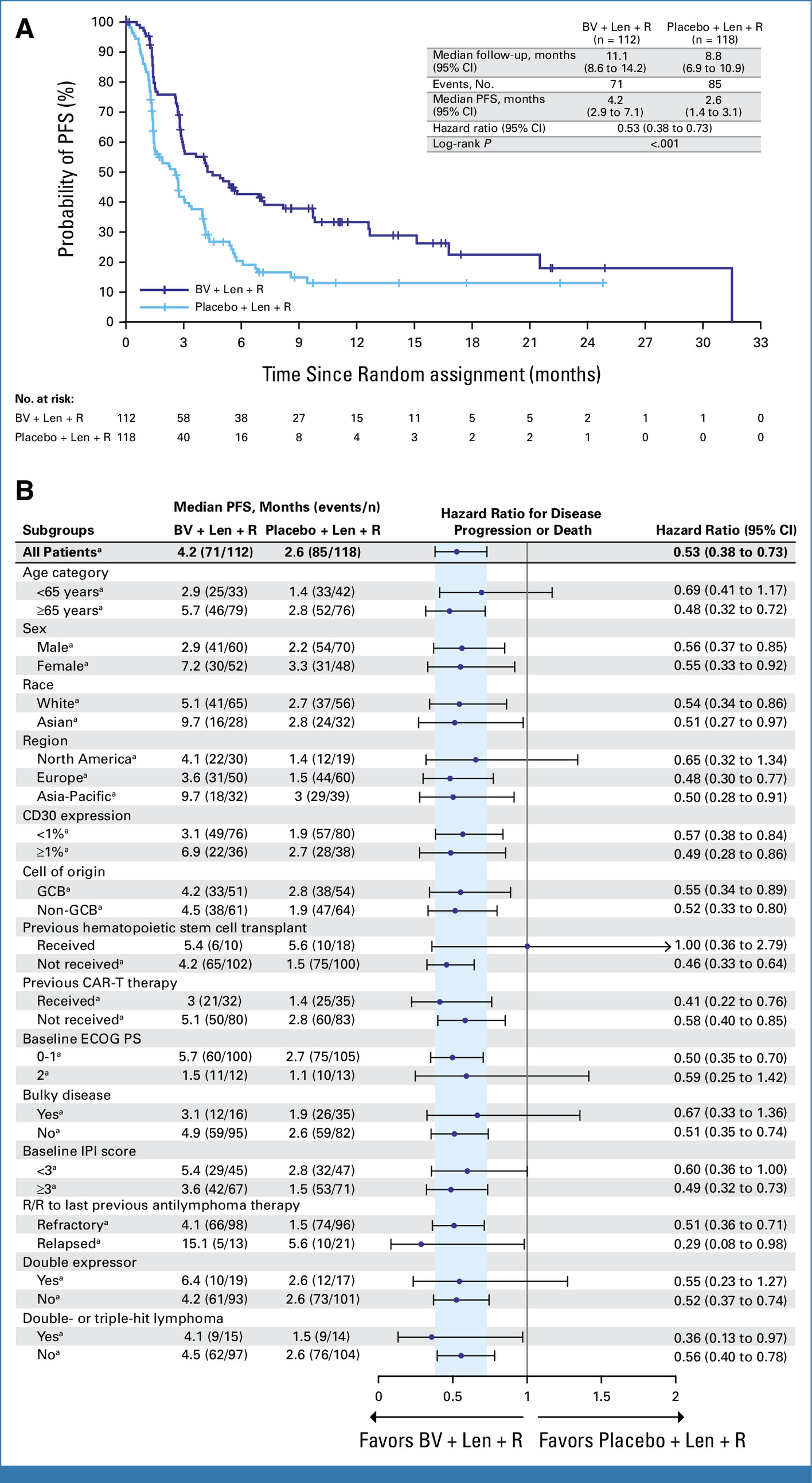
与安慰剂组相比,实验组显著降低了 47% 的疾病进展或死亡风险,中位无进展生存期分别为 4.2 个月和 2.6 个月。实验组完全缓解和部分缓解患者的中位 PFS 分别为 21.5 个月和 4.1 个月。
实验组客观缓解率为64%,安慰剂组为42%,中位缓解持续时间(DOR)分别为8.3 个月和3 个月。实验组的 CR 率高于安慰剂组(40%vs19%)。
ADCETRIS是一种抗体-药物偶联物(ADC),由CD30定向单克隆抗体组成,利用Pfizer的专有技术,通过蛋白酶可切割接头与微管破坏剂单甲基澳瑞他汀E (MMAE)连接。ADC 采用一种接头系统,该系统旨在在血液中稳定,但在内化到 CD30 阳性肿瘤细胞中时释放 MMAE。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-brentuximab-vedotin-lenalidomide-and-rituximab-relapsed-or-refractory-large-b-cell
2.https://ascopubs.org/doi/10.1200/JCO-24-02242?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed

相关推荐
随便看看
- 纳鲁索拜单抗针对不可切除或手术困难的骨巨细胞瘤的Ib/Ⅱ期临床研究亮相《nature communications》
- 什么是ADC药物
- 皮尔法伯实验室获得欧洲药品管理局人用药品委员会 (CHMP) 针对 BRAFTOVI®(康奈非尼)联合 MEKTOVI®(比美替尼)用于 BRAFV600E 突变晚期非小细胞肺癌 (NSCLC) 成人
- 欧盟十年来首个批准用于治疗转移性结直肠癌的创新靶向疗法-呋喹替尼
- casdatifan治疗透明细胞肾细胞癌1/1b 期研究显示出良好反应
- 苯甲酸安达替尼胶囊(PLB1004胶囊)拟纳入优先审评
- 肺癌治疗新突破!第四代EGFR抑制剂即将亮相,打破奥希替尼耐药困境
- 依沃西单药一线治疗PD-L1阳性非小细胞肺癌的新药上市申请获国家药品监督管理局受理
- 注射用维贝柯妥塔单抗拟纳入优先审评
- ADC药物德曲妥珠单抗DESTINY-Breast09 III期研究成果亮相2025 ASCO











