3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用JSKN003拟纳入突破性治疗,用于治疗铂耐药复发性上皮性卵巢癌、原发性腹膜癌或输卵管癌。

JSKN003是康宁杰瑞利用特有的糖基定点偶联平台自主研发的HER2双抗ADC,能够结合肿瘤细胞表面的HER2,通过细胞内吞释放拓扑异构酶Ⅰ抑制剂,进而发挥抗肿瘤作用。JSKN003较同类ADC药物具有更好的血清稳定性、更强的旁观者杀伤效应,有效地扩大了治疗窗。
2024年欧洲肿瘤内科学会(ESMO)大会上公布了HER2双抗偶联药物JSKN003治疗铂耐药卵巢癌患者:两项研究的汇总分析。JSKN003-101(NCT05494918)是一项在澳大利亚晚期/转移性实体瘤患者中进行的剂量递增和剂量扩展的Ⅰ期临床研究,JSKN003-102(NCT05744427)是一项在中国晚期实体瘤患者中进行的Ⅰ期(剂量递增和剂量扩展)和Ⅱ期(队列扩展)临床研究。两项研究汇总分析了JSKN003治疗铂耐药卵巢癌患者的安全性和疗效。
50例铂耐药卵巢癌患者接受了JSKN003治疗,在44例有至少一次基线后肿评的患者中,客观缓解率(ORR)为56.8%,39例患者(88.6%)出现肿瘤缩小。经中心实验室确认的HER2 IHC 0和有HER2表达(IHC 1+、2+和3+)的患者中,ORR分别为52.9%和68.8%。33例接受过贝伐珠单抗治疗的患者,ORR为54.5%(95% CI:36.4, 71.9);26例接受过PARP抑制剂治疗的患者,ORR为46.2%。
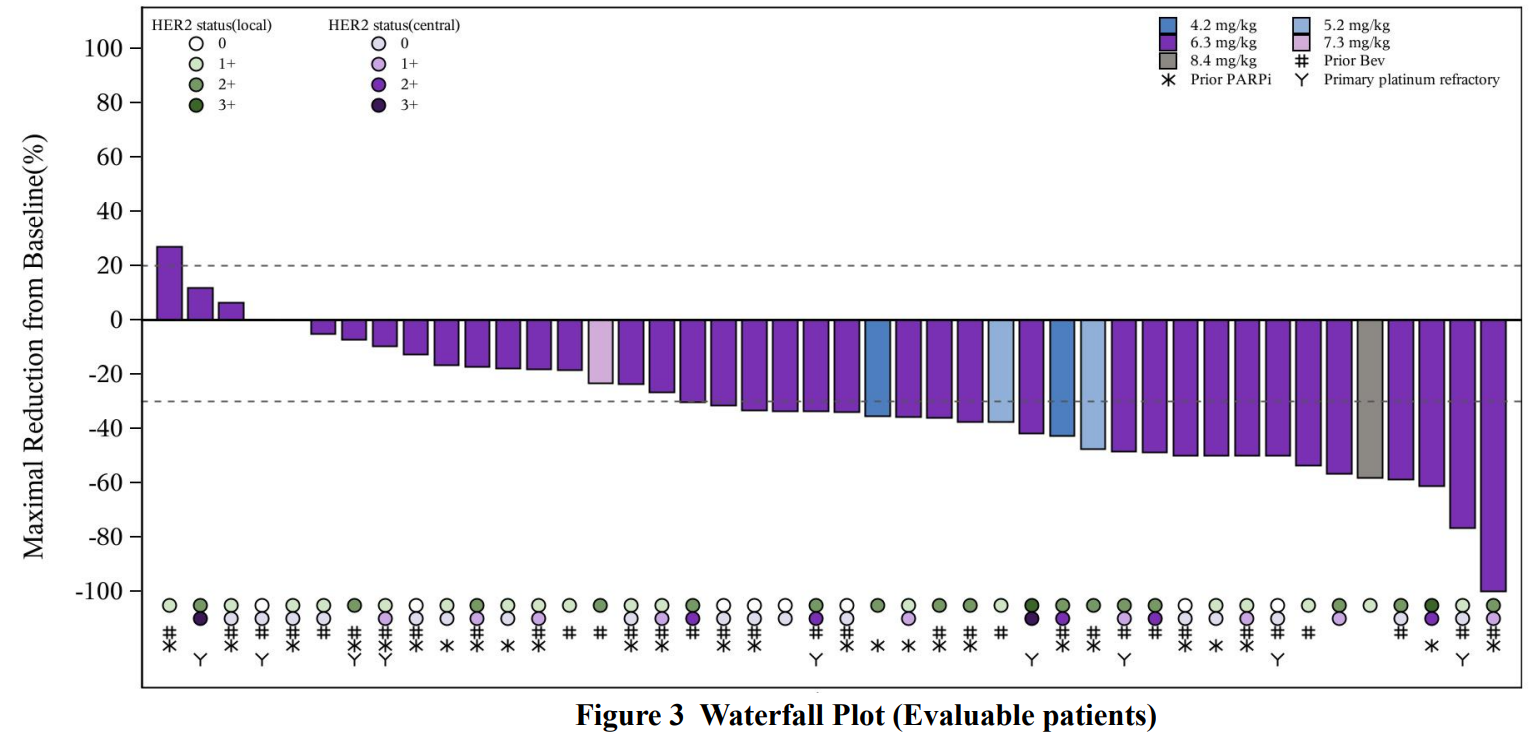
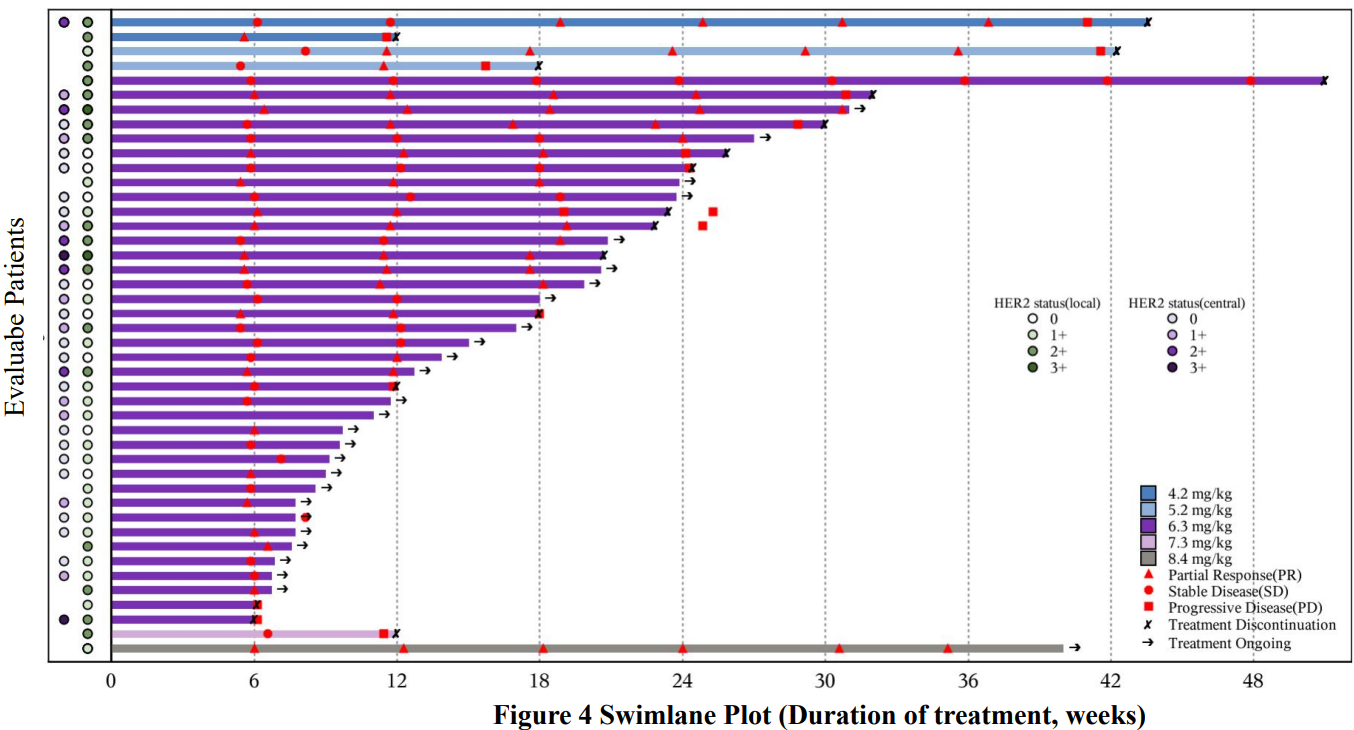
截图源于参考资料2
该会议同样公布了JSKN003治疗晚期HER2阳性(IHC 3+)实体瘤(乳腺癌除外)患者的临床数据,此次在ESMO大会上公布了澳大利亚Ⅰ期临床研究JSKN003-101(NCT05494918)和中国Ⅰ/Ⅱ期临床研究JSKN003-102(NCT05744427)中,治疗经组织学证实为HER2阳性(IHC 3+)实体瘤的汇总分析结果。
截至2024年7月15日,29例患者(结直肠癌:9例、胃癌:6例、胆道癌:4例、食管癌:3例、卵巢癌:2例、头颈癌:1例和其他癌症:4例)入组,28例患者可进行疗效分析,客观缓解率(ORR)和疾病控制率(DCR)分别为75.0%和89.3%。在7例接受过抗HER2 ADC治疗的患者中,ORR为71.4%。胃癌和结直肠癌的ORR分别为83.3%(5/6)和66.7%(6/9)。
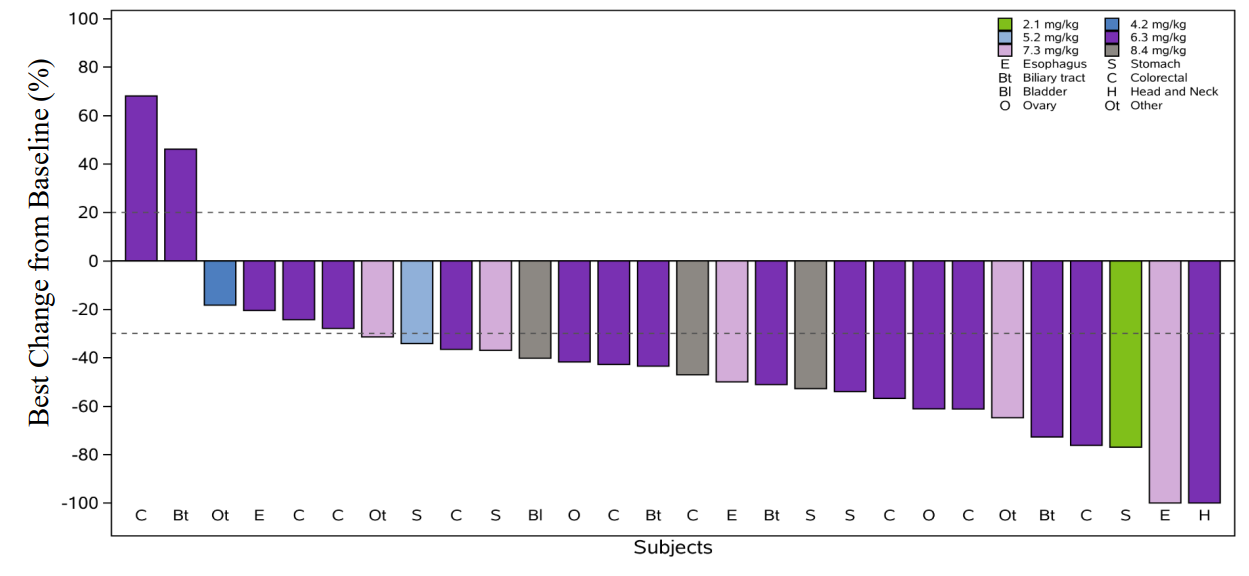
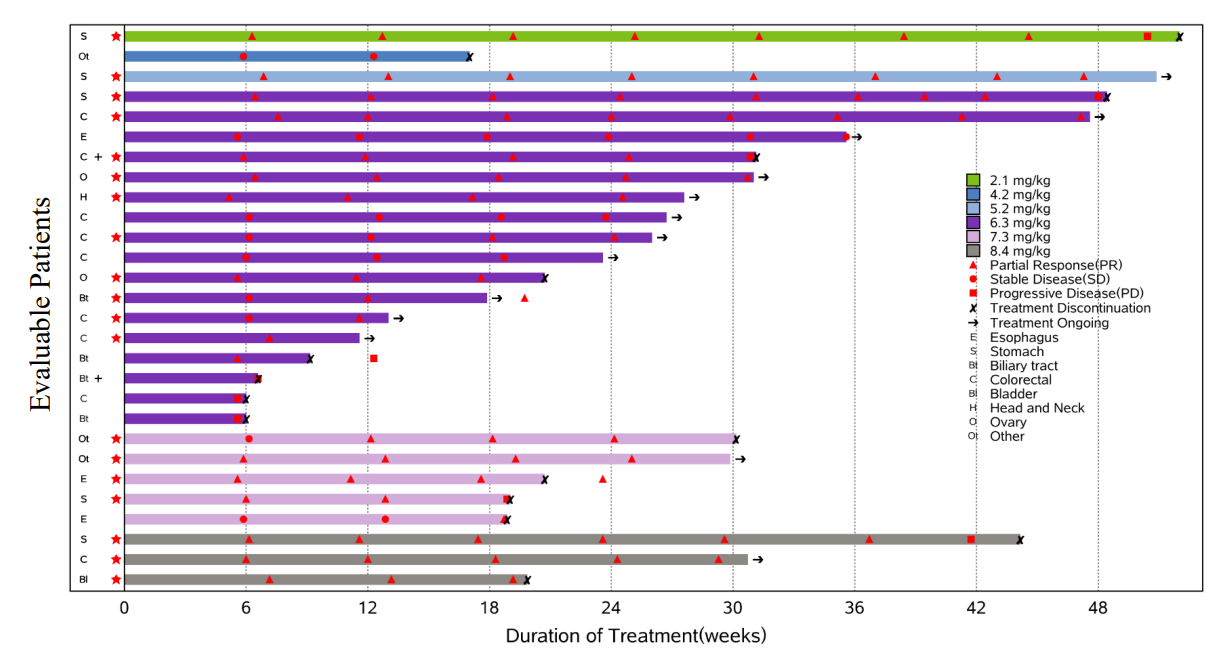
截图源于参考资料2
目前ADC药物有临床试验正在寻找胃癌、乳腺癌、头颈癌等患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.alphamabonc.com/uploads/images/172640044276681.pdf
2.https://www.alphamabonc.com/uploads/images/172640058227946.pdf

相关推荐
随便看看
- HS-20093(B7-H3 ADC)用于复发或难治性肉瘤治疗的II期研究结果入选2025年欧洲肿瘤内科学会(ESMO)年会
- 皮尔法伯实验室获得欧洲药品管理局人用药品委员会 (CHMP) 针对 BRAFTOVI®(康奈非尼)联合 MEKTOVI®(比美替尼)用于 BRAFV600E 突变晚期非小细胞肺癌 (NSCLC) 成人
- 舒格利单抗获欧盟委员会批准用于一线治疗非小细胞肺癌
- 抗CD20/CD3双抗JS203即将亮相2025 ASH大会
- 客观缓解率达74%!肺癌第四代ALK抑制剂来了,恩沙替尼上市许可申请获受理
- 注射用ATG-022 ADC拟纳入突破性治疗
- OS Therapies宣布OST-HER2治疗骨肉瘤2年生存率达75%
- ADC药物-YL201让晚期实体瘤患者“柳暗花明”,在多种癌症治疗中大放异彩
- 亚盛医药APG-2575拟纳入优先审评
- 特瑞普利单抗获得欧洲药品管理局人用药品委员会积极意见支持其用于晚期鼻咽癌和食管癌的一线治疗











