9月11日,石药集团宣布其与江苏康宁杰瑞合作开发的KN026(安尼妥单抗注射液)的新药上市申请已获国家药品监督管理局受理,适应症为联合化疗用于至少接受过一种系统性治疗(必须包含曲妥珠单抗联合化疗)失败,HER2阳性局部晚期、复发或转移性的胃/胃—食管结合部腺癌。

该产品是一种抗HER2双特异性抗体,可同时结合HER2的两个非重叠表位,导致HER2信号阻断。在2024年欧洲肿瘤内科学会(ESMO)大会上,该产品的II期临床研究结果首次公布。该研究结果显示,该产品联合化疗的客观缓解率为40.0%,经独立评审委员会(IRC)评估的中位无进展生存期为8.6个月,中位总生存期为13.2个月。本次上市申请主要是基于一项关键II/III期临床试验(KC-WISE)。III期临床研究的首次期中分析结果显示,与目前的标准治疗相比,该产品联合化疗可显著提高临床疗效,延长无进展生存期和总生存期,且在安全性方面无新发安全性风险,心脏毒性发生率低,免疫原性低。
2025年3月19日,《Signal Transductionand Targeted Therapy》发表了KN026联合KN046在晚期HER2阳性实体瘤中的抗肿瘤活性。
入组了149名患者(Ib期47例,II期102例),肿瘤类型包括GC(n = 74)、结直肠癌(CRC)(n = 26)和其他实体瘤(n = 13)。
共有108名患者完成了疗效评估,在所有接受评估的患者中,60例患者达到客观缓解(完全缓解[CR],n=1;部分缓解[PR],n=59),30例患者疾病稳定(SD)。总体客观缓解率(ORR)为55.6%,疾病控制率(DCR)为83.3%,临床获益率(CBR)为61.1%。
在既往接受过治疗(pretreated)的HER2阳性患者(n=61)中,27例曾接受过抗HER2治疗,其中14例(51.9%)达到PR。在接受过PD-1/PD-L1阻断治疗(n=15)的患者中,9例(60.0%)达到PR。在同时接受过抗HER2治疗和PD-1/PD-L1阻断治疗(n=6)的患者中,仍有4例(66.7%)观察到客观缓解。
在Ib期研究中,最初纳入了HER2阳性、低表达及突变状态的患者,以探索安全性及潜在获益人群。客观缓解仅见于HER2阳性患者。此外,与HER2低表达或突变患者相比,HER2阳性患者的中位无进展生存期(PFS)相对更长(6.2个月 vs. 3.6个月),中位总生存期(OS)也较长(未达到[NE] vs. 13.4个月)。因此,后续研究仅纳入HER2阳性实体瘤患者。
在HER2阳性胃癌(GC)亚组中,11例接受该方案作为二线治疗的患者中,有7例(63.5%)达到PR,其中5例(45.5%)为确认性PR。鉴于二线治疗的良好疗效,在数据安全监查委员会(DSMC)讨论后,进一步入组了初治的晚期HER2阳性GC患者。在这7例初治患者中,有6例(85.7%)达到PR。因此,在II期研究中进一步探索了该方案用于一线治疗的可行性。
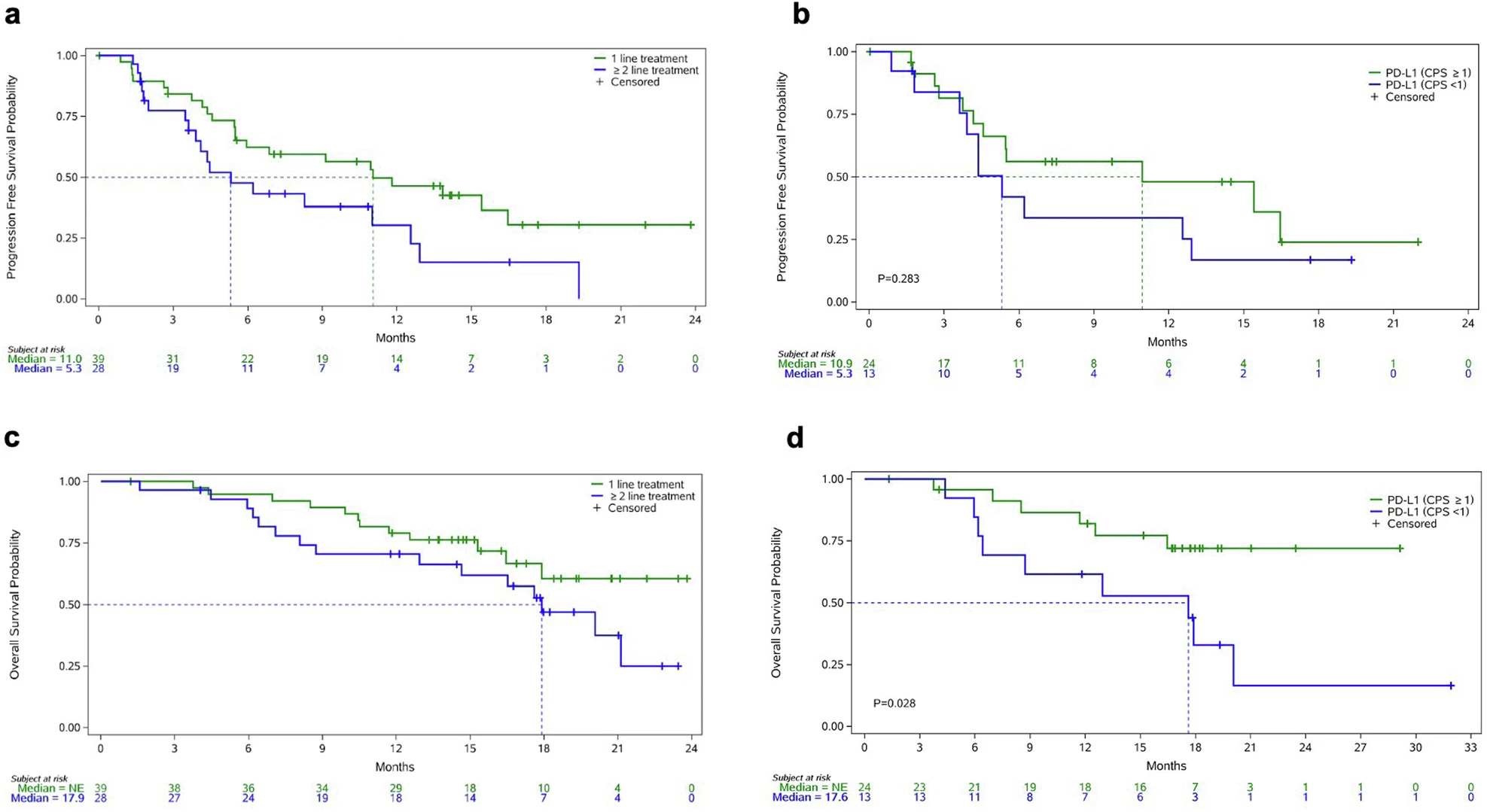
最终,共有38例HER2阳性GC患者(来自Ib期和II期研究)接受了该方案作为一线治疗。其中30例患者达到客观缓解(CR,n=1;PR,n=29),ORR和DCR分别为78.9%和89.5%。仅3例患者在首次疗效评估时出现疾病进展(。中位缓解持续时间(DoR)为13.4个月,中位PFS为11.0个月,中位OS尚未达到。
此外,另有27例HER2阳性GC患者接受了KN026联合KN046作为≥二线治疗。其中12例达到PR,11例为SD,ORR为44.4%,DCR为85.2%。中位DoR为10.8个月,中位PFS为5.3个月。

临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 超90%的患者病情得到控制!EGFR靶向药展现超强疗效,抗击肺癌
- 特瑞普利单抗用于肝细胞癌新适应症上市申请获受理
- 胃癌/卵巢癌患者速看!ADC药物JSKN003获FDA孤儿药资格,91%患者肿瘤缩小
- 再传佳音!我国自主研发药物呋喹替尼于香港获批用于治疗转移性结直肠癌,疾病控制率达62.2%
- 维迪西妥单抗实现HER2阳性乳腺癌患者肿瘤缩小!并拟纳入优先审评
- IMM2510联合化疗一线治疗非小细胞肺癌(NSCLC)患者的II期试验公布
- ADC药物注射用博度曲妥珠单抗获批上市
- 美国FDA授予Namodenoson(CF102)孤儿药资格认定,用于治疗胰腺癌
- 靶向CLDN18.2的ADC药物SHR-A1904治疗晚期胃癌或胃食管结合部癌(GC/GEJC)的研究数据登《Nature Medicine》
- 注射用德曲妥珠单抗在中国申报的第五个乳腺癌适应症的上市申请获得受理











