2月2日,国家药品监督管理局(NMPA)正式批准芦康沙妥珠单抗(Sac-TMT)新适应症,用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性(IHC 0、IHC 1+或IHC 2+/ISH-)乳腺癌成人患者。

OptiTROP-Breast02是一项在我国开展的多中心、随机对照、开放标签III期临床研究(NCT06081959),旨在评估芦康沙妥珠单抗相较于研究者选择的化疗(TPC,含艾立布林、长春瑞滨、吉西他滨和卡培他滨)治疗既往在任何疾病阶段接受过≥1种内分泌治疗(含≥1种CDK4/6抑制剂治疗且失败),且在晚期或转移性阶段接受过其它系统治疗、在任何阶段接受过紫杉烷类治疗的不可切除局部晚期或转移性HR+/HER2-乳腺癌患者的有效性和安全性。
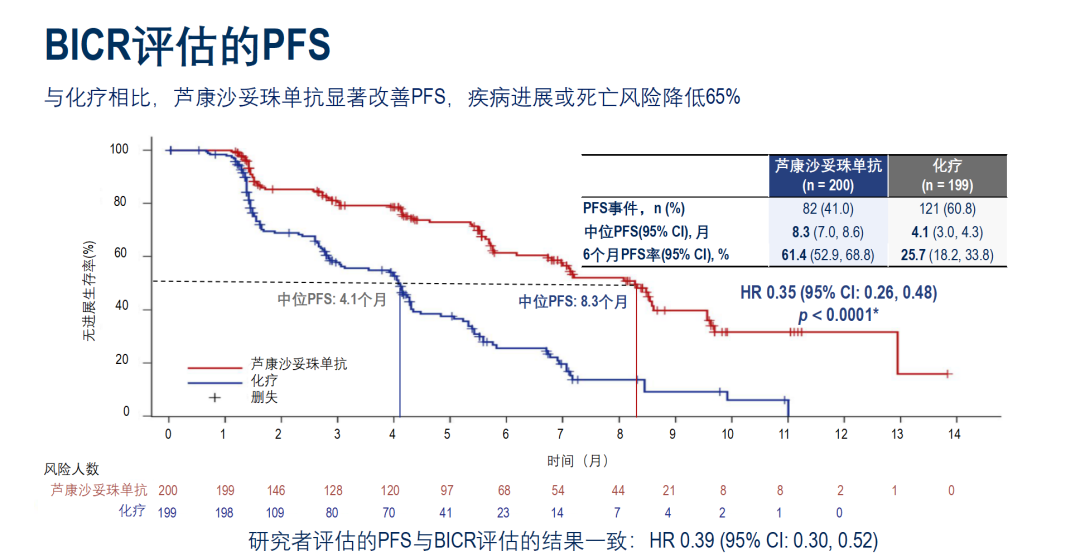
2025年ESMO大会上公布的OptiTROP-Breast02研究结果显示:芦康沙妥珠单抗显著延长了患者的PFS(8.3个月vs. 化疗组为4.1个月),疾病进展或死亡风险降低65%,且研究者与盲态独立中心审查(BICR)评估结果一致;亚组分析发现无论HER2表达如何,PFS获益一致,ORR达41.5%,均显著优于化疗组。在本次PFS期中分析时,已观察到芦康沙妥珠单抗积极的OS获益趋势。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找癌症患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 芦康沙妥珠单抗拟纳入优先审评,用于EGFR突变非小细胞肺癌成人患者
- 重磅!AK112治疗实体瘤研究结果出炉!疾病控制率达63.8%!
- 他雷替尼治疗ROS1阳性非小细胞肺癌死亡风险降低66%
- 颅内客观缓解率高达90.9%!新型ALK/ROS1抑制剂伊鲁阿克疗效数据出炉,治疗非小细胞肺癌患者疗效惊艳
- 绿叶制药小细胞肺癌创新药赞必佳®(注射用芦比替定)获批上市
- 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 美国FDA批准inavolisib用于乳腺癌
- AK104注射液拟纳入突破性治疗
- 中位缓解持续近4年!EGFR突变的非小细胞肺癌治疗新方案,特泊替尼联合奥希替尼最新结果!
- 安尼妥单抗注射液拟纳入优先审评











