2月5日,国家药品监督管理局 (NMPA)批准适加坦®(富马酸吉瑞替尼片)用于治疗采用经充分验证的检测方法检测到携带FMS样酪氨酸激酶3(FLT3)突变的复发性或难治性急性髓系白血病(AML)成人患者。

此次批准是基于 COMMODORE 的研究结果。COMMODORE(NCT03182244)是一项在FLT3突变型复发性或难治性 AML患者中比较吉瑞替尼与补救性化疗的开放性、多中心、随机、Ⅲ期研究。2024年9月5日,《Leukemia》发表了该试验数据。
结果显示:234 名患者被随机分组,116例纳入吉瑞替尼组,118例纳入对照组,吉替替尼组中位总生存期(PFS)为 11.2 个月,对照组为 8.1 个月。1 年生存率分别为 35.1% 和 25.1%。
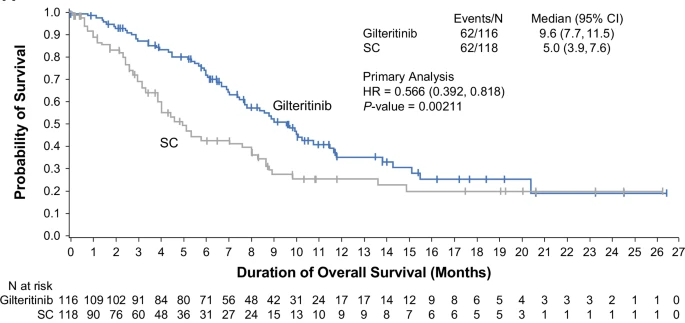
吉替替尼组19例患者达到完全缓解(CR),18例患者部分缓解(PR),对照组12例患者完全缓解(CR),6例患者部分缓解(PR)。吉替替尼组无事件生存率(EFS)较对照组显著延长。
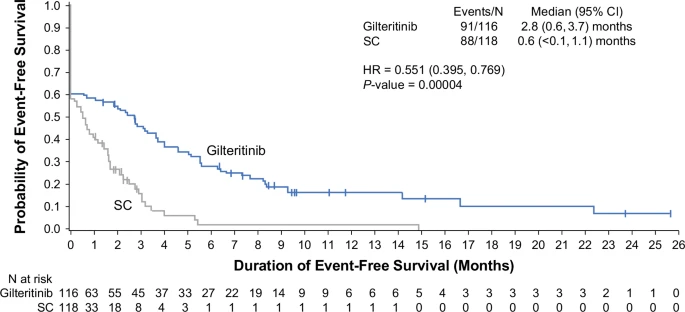
吉瑞替尼是一种类 FMS 样酪氨酸激酶 3 (FLT3) 抑制剂,具有抗 FLT3-ITD(一种常见驱动突变,具有高疾病负担以及不良预后)和 FLT3-TKD 突变的活性。
急性髓系白血病(AML)是一种异质性血液系统恶性肿瘤,尤其对于携带不良预后突变(比如FLT3)的患者,长期以来一直是临床治疗中的重大挑战。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.nature.com/articles/s41375-024-02382-9

相关推荐
随便看看
- 美国FDA批准inavolisib用于乳腺癌
- 伯瑞替尼治疗携带 c-Met 改变的局部晚期或转移性非小细胞肺癌患者的II期KUNPENG 临床试验数据公布
- 依沃西单抗纳入突破性治疗
- 枸橼酸戈来雷塞片获批上市,用于KRAS G12C突变非小细胞肺癌
- 菲诺利单抗获批一线治疗头颈部鳞状细胞癌
- 注射用BL-B01D1拟纳入优先审评
- ADC药物SHR-A1921治疗铂耐药卵巢癌的首次人体I期研究数据亮相ESMO
- 美国FDA批准开展JS207新辅助治疗非小细胞肺癌的Ⅱ/Ⅲ期临床研究
- 恩沃利单抗联合疗法在微卫星稳定/错配修复功能正常(MSS/pMMR)的结直肠癌患者中显示出积极效果
- 美国FDA授予Namodenoson(CF102)孤儿药资格认定,用于治疗胰腺癌











