热门推荐
- 精 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- 精 疾病控制率高达90.9%!KRAS G12C抑制剂出击结直肠癌、非小细胞肺癌!
- 精 重磅!“治愈”肺癌更进一步!ALK抑制剂阿来替尼无病生存率高达93.8%!
- 精 85%患者的病情得到控制!KRAS G12C突变的患者有前景的治疗选择
- 精 HER2阳性实体瘤患者命运将改写!DS-8201再获FDA批准,不限癌种!
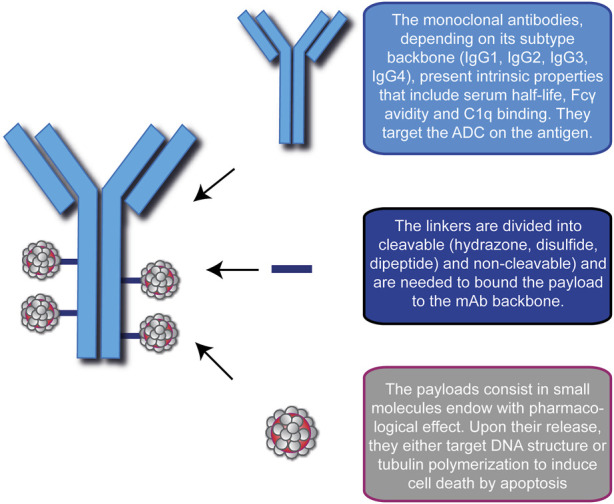
- 精 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 精 复发风险降低60%!特瑞普利单抗注射液再填适应症,我国首个、全球第二个获批的肺癌围手术期疗法
- 精 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 精 NTRK融合让众多实体瘤战栗,成为击败肿瘤的重磅武器
- 精 奥布替尼(Orelabrutinib)广受认可,让更多血液系统肿瘤患者获益
- 精 首款RET抑制剂普拉替尼给非小细胞肺癌患者带来希望
- 精 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款
- 精 收藏 | 不能错过的胃癌的药物治疗大全!
- 精 KRAS基因靶点药物不间断研究中
- 精 仑伐替尼一种重要的靶向药
- 精 “不完美心动”——干细胞叫嚣“心衰”
- 精 伏美替尼 (Furmonertinib)第三代EGFR-TKI强势来袭
- 精 一文教会你BRCA突变和PAPR抑制剂的关系
- 精 国家药监局批准三款新药上市!!!攻克癌症不再天方夜谭!
- 精 中国首款自主研发的CAR-T细胞治疗伊基奥伦赛注射液获批上市
- 精 培美曲塞
资讯列表
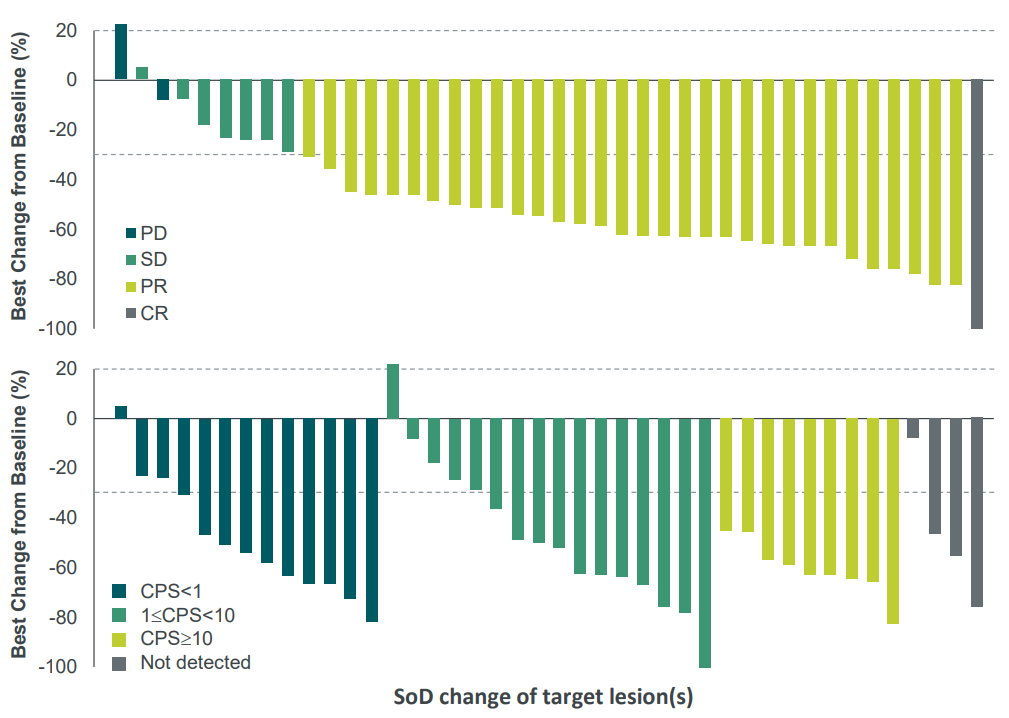
近日,《Signal Transduction and Targeted Therapy》发表了安罗替尼联合派安普利单抗联合化疗用于IIB-IIIB期非小细胞肺癌(NSCLC)患者围术期治疗的三臂前瞻性临床试验研究。
2月3日,拜耳宣布国家药品监督管理局(NMPA)正式批准口服新型雄激素受体抑制剂(ARi)诺倍戈®(达罗他胺片)联合雄激素剥夺疗法(ADT)治疗转移性激素敏感性前列腺癌(mHSPC)成年患者。诺倍戈®此前已先后获批用于治疗有高危转移风险的非转移性去势抵抗性前列腺癌(NM-CRPC)成年患者,和联合多西他赛治疗转移性激素...
1月29日,国家药品监督管理局药品审评中心(CDE)显示:康方生物自主研发的全球首创双特异性抗体新药依沃西单抗(AK112)拟纳入突破性治疗,联合吉西他滨和顺铂一线治疗晚期胆道癌。
1月29日,国家药品监督管理局药品审评中心(CDE)显示:恒瑞医药申请的HRS-4642注射液拟纳入突破性治疗,用于联合吉西他滨和紫杉醇(白蛋白结合型)用于携带KRAS G12D突变的晚期或转移性胰腺癌的一线治疗。
1月21日,《新英格兰医学杂志》发表了一项突破性临床研究结果:抗体偶联药物(ADC)戈沙妥珠单抗联合帕博利珠单抗一线治疗PD-L1阳性转移性三阴乳腺癌,将患者无进展生存期从7.8个月延长至11.2个月,客观缓解率达到60%,其中13%的患者达到了完全缓解(CR)。更关键的是,对于起效的患者,中位缓解持续时间长达16.5...
1月28日,国家药品监督管理局药品审评中心(CDE)显示:注射用PRO1184拟纳入突破性治疗品种,治疗既往接受过系统性治疗的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者。
1月28日,国家药品监督管理局药品审评中心(CDE)显示:注射用瑞康曲妥珠单抗拟纳入优先审评,适用于经奥沙利铂、氟尿嘧啶和伊立替康治疗失败的HER2阳性结直肠癌成人患者。
1月27日,美国食品药品监督管理局(FDA)批准达雷妥尤单抗注射液(Daratumumab)与透明质酸酶 - fihj(hyaluronidase-fihj)联合化疗用于新诊断的多发性骨髓瘤成人,且不符合自体干细胞移植(ASCT)资格。